通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是( )
| |
操作、现象 |
解释 |
| A |
向KI-淀粉溶液中加入FeCl3溶液,溶液变蓝 |
Fe3+能与淀粉发生显色反应 |
| B |
把生铁放置于潮湿的空气中,铁表面有一层红棕色的斑点 |
铁在潮湿的空气中易生成Fe(OH)3 |
| C |
向稀硝酸中加入少量铁粉,有气泡产生 |
说明Fe置换出硝酸中的氢,生成了氢气 |
| D |
新制Fe(OH)2露置于空气中一段时间,白色物质变成了红褐色 |
说明Fe(OH)2易被O2氧化成Fe(OH)3 |
若锌与稀硝酸反应时,其化学反应方程式为
4Zn+10HNO3=aZn(NO3)2+bM+cH2O,则a、b、c、M可能分别为()
| A.4、1、5、N2O | B.4、2、4、NO2 |
| C.4、1、3、NH4NO3 | D.4、3、5、NO |
在一定条件下,PbO2与Cr3+反应,产物是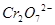 和
和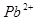 ,则参加反应的
,则参加反应的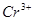 与
与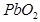 的个数之比为()
的个数之比为()
| A.1:3 | B.2:3 | C.1:1 | D.4:3 |
密度为0.91 g·cm-3的氨水,质量百分比浓度为25%(即质量分数为0.25),该氨水用等体积的水稀释后,所得溶液的质量百分比浓度
| A.等于12.5% | B.大于12.5% | C.小于12.5% | D.无法确定 |
下列叙述中正确的是是()
| A.氢氧根离子的摩尔质量是17g |
| B.每mol硫酸所含硫酸的分子数为6.02×1023/mol |
| C.物质的量浓度相同的溶液中,所含溶质的微粒数相同 |
| D.0.1 mol氯化氢约含有6.02×1022个氯化氢分子 |
下列说法正确的是(N0表示阿伏加德罗常数的值)
| A.在常温常压下,11.2 L N2含有的分子数为0.5 N0 |
| B.在常温常压下,1 mol Ne含有的原子数为N0 |
| C.71 g Cl2所含原子数为2N0 |
| D.在同温同压时,相同体积的任何气体单质所含的原子数相同 |