V、W、X、Y均是元素周期表中短周期元素,在周期表中的相对位置关系如表所示:
| |
Y |
V |
|
|
| X |
|
|
|
W |
Z为第四周期常见元素,该元素是人体血液中血红蛋白最重要的组成金属元素。V的最简单氢化物为甲,W的最简单氢化物为乙,甲、乙混合时有白烟生成。下列说法正确的是( )。
A.原子半径:X>Y>V>W
B.X、W的质子数之和与最外层电子数之和的比值为2∶1
C.甲、乙混合时所生成的白烟为离子化合物,但其中含有共价键
D.少量Z的单质与过量W的单质可化合生成ZW2
某反应过程中体系的能量变化如图所示,下列说法错误的是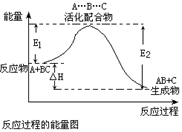
| A.反应过程可表示为 A+BC—→[A…B…C] —→AB+C (反应物)(过渡态)(产物) |
| B.此图中逆反应的热效应△H=E1—E2,为吸热反应 |
| C.正反应的热效应为△H=E1—E2,且E2>E1,所以正反应为放热反应 |
| D.E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能 |
在体积一定的密闭容器中给定物质A、B、C的量,在一定条件下
发生反应建立的化学平衡:aA(g) + bB(g) xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指
xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指
A.反应物A的百分含量 B.平衡混合气中物质B的百分含量
C.平衡混合气的密度 D.平衡混合气的平均摩尔质量
对于可逆反应N2(g)+3H2(g) 2NH3(g);△H<0,下列研究目的和示意图相符的是
2NH3(g);△H<0,下列研究目的和示意图相符的是
下列事实不能用勒夏特列原理解释的是
| A.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| B.光照氯水,颜色变浅 |
| C.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的转化率 |
| D.由H2、I2(g)、HI组成的平衡体系,加压后颜色加深 |
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g) Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
| A.达到平衡时,X与Y 的浓度相等 |
| B.将容器体积变为20 L,Z的平衡浓度变为原来的1/2 |
| C.若升高温度Y的转化率减小,则正反应为吸热反应 |
| D.以X浓度变化表示的反应速率为0.001 mol/(L·s) |