几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
X |
Y |
Z |
W |
| 原子半径/10-12 m |
160 |
110 |
70 |
66 |
| 主要化合价 |
+2 |
+5、+3、-3 |
+5、+3、-3 |
-2 |
下列叙述正确的是 ( )。
A.离子半径:W<X
B.气态氢化物的稳定性:Z>W
C.化合物X3Z2中既含有离子键又含有共价键
D.最高价氧化物对应水化物的酸性:Z>Y
下列有关生活中的化学的叙述中错误的是
①向燃料煤中加入生石灰,可以减少对大气的污染
②用双氧水清洗伤口,可以杀菌消毒
③只用淀粉溶液就能检验出食盐中是否加碘
④使用明矾可以对饮用水进行消毒、杀菌
⑤硫酸钡是一种难溶于水、难溶于酸的盐,可用作X光透视肠胃的内服药剂
| A.①③④ | B.①②⑤ | C.③④ | D.③④⑤ |
铁和氧化铁的混合物共x mol,加盐酸后固体全部溶解,共收集到ymol氢气,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中铁的物质的量为( )
A.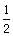 (x-y) mol (x-y) mol |
B.(x-y) mol | C.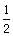 (x+y)mol (x+y)mol |
D.(x+y) mol |
某含铬Cr2O72- 废水用硫酸亚铁铵[FeSO4·(NH4)2 SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀干燥后得到n molFeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述正确的是
| A.消耗硫酸亚铁铵的物质的量为n(2-x)mol |
| B.处理废水中Cr2O72- 的物质的量为nxmol |
| C.反应中发生转移的电子数为3n mol |
| D.在FeO·FeyCrxO3中3x=y |
200℃时,11.6 g CO2和水蒸气的混合气体与过量的Na2O2充分反应后,固体质量增加了3.6 g,再将反应后剩余固体冷却后加入含有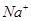 、
、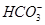 、
、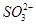 、
、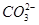 等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是 ( )
等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是 ( )
| A.原混合气体的平均摩尔质量为23.2 g/mol |
| B.混合气体与Na2O2反应过程中电子转移的物质的量为0.25 mol |
C.溶液中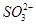 的物质的量浓度基本保持不变 的物质的量浓度基本保持不变 |
D.溶液中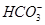 的物质的量浓度减小, 的物质的量浓度减小,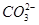 的物质的量浓度增大,但是 的物质的量浓度增大,但是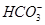 和 和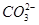 的物质的量浓度之和基本保持不变 的物质的量浓度之和基本保持不变 |
下列反应所得溶液中一定只含一种溶质的是( )
| A.向AlCl3溶液中加入过量NaOH溶液 |
| B.向NaOH溶液中通入CO2气体 |
| C.向MgSO4、H2SO4的混合溶液中加入过量的Ba(OH)2溶液 |
| D.向NaHCO3溶液中加入CaC2固体 |