利用硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下: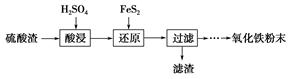
(1)“酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率;②________。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO42—,该反应的离子方程式为________________________________________________________________________。
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入稀盐酸、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应的化学方程式如下:
2Fe3++Sn2++6Cl-=2Fe2++SnCl62—
Sn2++4Cl-+2HgCl2=SnCl62—+Hg2Cl2↓
6Fe2++Cr2O72—+14H+=6Fe3++2Cr3++7H2O
①若SnCl2不足量,则测定的Fe3+量________(填“偏高”、“偏低”或“不变”,下同);
②若不加HgCl2,则测定的Fe3+量________。
(4)①可选用________(填试剂)检验滤液中含有Fe3+。产生Fe3+的原因是________________________________________________________________________(用离子方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Fe(OH)2 |
Mg(OH)2 |
Mn(OH)2 |
| 开始沉淀 |
2.7 |
3.8 |
7.5 |
9.4 |
8.3 |
| 完全沉淀 |
3.2 |
5.2 |
9.7 |
12.4 |
9.8 |
实验可选用的试剂有:稀硝酸、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。
请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a.氧化:________________________________________________________;
b.沉淀:__________________________________________________________;
c.分离,洗涤;
d.烘干,研磨。
二氧化碳“组合转化”的某烷烃碳架结构如图所示: ,此烷烃的一溴代物有种;若此烷烃为炔烃加氢制得,则此炔烃的结构简式为,
,此烷烃的一溴代物有种;若此烷烃为炔烃加氢制得,则此炔烃的结构简式为,
在乙醇的化学性质中,各反应的断键方式可概括如下: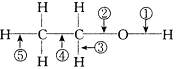
⑴消去反应:;⑵与金属反应:;
⑶催化氧化:;⑷分子间脱水:;
⑸与HX反应:。
莽草酸的结构式如图: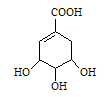 ,请回答:
,请回答:
(1)写出莽草酸分子中官能团名称。
(2)该有机物分子1moL最多能和moL NaOH发生反应。
以下是以莽草酸A为原料的有机合成路线: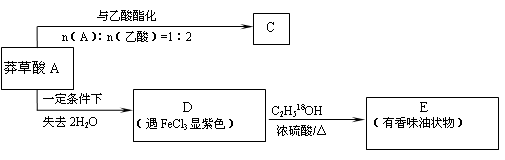
已知D的碳环上一氯代物只有两种。请继续回答下列问题:
(3)C有三种同分异构体,写出其中的一种结构简式。
(4)莽草酸A→D的反应类型是:。
(5)写出下列反应的化学方程式:
① D与足量的NaHCO3溶液反应;
② D→E。
根据下列的有机物合成路线回答问题: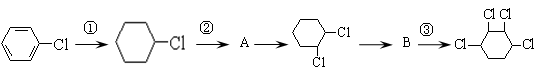
(1)写出A、B的结构简式:
A、B。
(2)写出各步反应类型:
①、②、③。
(3)写出②、③的反应方程式:
②,③。
(12分)今有化合物: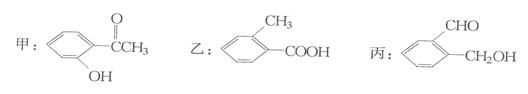
(1) 请判别上述哪些化合物互为同分异构体:。
(2) 请分别写出鉴别甲、乙的方法。(指明所选试剂及主要现象即可)
鉴别甲的方法:;
鉴别乙的方法:;
(3)鉴别丙的方法可以让其与银氨溶液反应,请写出该反应的化学方程式:。
(4)请按酸性由强至弱排列甲、乙、丙的顺序:。