决定化学反应速率的根本因素是
| A.温度和压强 | B.反应物的浓度 |
| C.参加反应的各物质的性质 | D.催化剂的加入 |
下面关于SiO2晶体网状结构的叙述正确的是
| A.最小的环上,有3个Si原子和3个O原子 |
| B.最小的环上,Si和O原子数之比为1﹕2 |
| C.最小的环上,有6个Si原子和6个O原子 |
| D.存在四面体结构单元,O处于中心,Si处于4个顶角 |
A、B、C为三种短周期元素,A、B在同周期, A、C的最低价离子分别为A2-和C-B2+和C-具有相同的电子层结构。下列说法中正确的是
A.原子序数:A>B>C B.原子半径:A>B>C
C.离子半径:A2->C->B2+ D.原子核外最外层电子数:A>C>B
下列说法正确的是:()
| A.仅含有Na+、H+、OH—、CH3COO—四种离子的某溶液中可能存在: c(Na+)>c(OH—)>c(CH3COO—)>c(H+) |
| B.铝热法炼铁过程中镁条和氯酸钾起催化作用 |
| C.二氧化硫的催化氧化是放热反应,升高温度可以减慢该反应的速率 |
| D.人体内淀粉、脂肪、蛋白质的水解都是由酶所催化的 |
已知反应:①Cl2+2KBr=2KCl+Br2②K ClO3+6HCl=3Cl2+KCl+3H2O
ClO3+6HCl=3Cl2+KCl+3H2O
③ 2KBrO3+Cl2=Br2+2KClO3,下面说法正确的
| A.上述三个反应都有单质生成,所以都是置换反应 |
| B.反应②中还原剂与氧化剂的物质的量之比为6:1 |
| C.反应③中1mol Cl2反应,则氧化剂得电子的物质的量为10mol |
| D.氧化性由强到弱的顺序为:KClO3>KBrO3>Cl2>Br2 |
用下列装置不能达到有关实验目的的是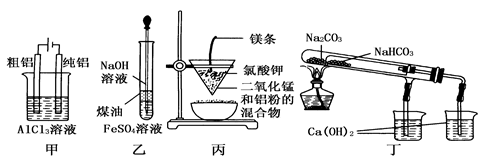
| A.用甲图装置电解精炼铝 |
| B.用乙图装置制备Fe(OH)2 |
| C.用丙图装置可制得金属锰 |
| D.用丁图装置验证NaHCO3和Na2CO3的热稳定性 |