氯化铵简称“氯铵”,又称卤砂,为无色晶体或白色结晶性粉末,易溶于水中,在工农业生产中用途广泛。以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
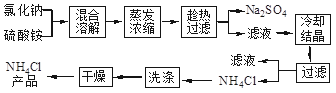
氯化铵和硫酸钠的溶解度随温度变化如图所示。回答下列问题:
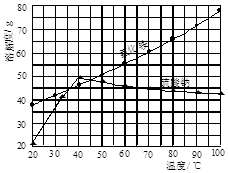
(1)实验室进行蒸发浓缩用到的主要仪器有 、烧杯、玻璃棒、酒精灯等。
(2)实验过程中趁热过滤的目的是 。
(3)写出“蒸发浓缩”时发生的化学方程式: 。
(4)某研究性学习小组为测定该NH4Cl产品中氮的含量,设计了如图装置,并进行了讨论。

甲同学:根据此实验测得的数据,计算的NH4Cl产品的含氮量可能偏高,因为实验装置中存在一个明显缺陷是: ____ 。
乙同学:实验过程中,往烧瓶中加入的浓氢氧化钠溶液的离子反应方程式为 ,反应过程中NaOH一定要足量并充分加热,原因是 。
用改进后的实验装置重新进行实验,称取13.0gNH4Cl产品,测得实验后B装置增重3.4g。则该化肥含氮量为 。
(6分)某种白色晶体A与盐酸反应,产生无刺激性气味、可使澄清石灰水变浑浊的气体B,若在A的水溶液中加氢氧化钡溶液,并稍微加热,则析出白色沉淀C和无色气体D,D可使湿润的红色石蕊试纸变蓝;加热固体A可生成水、B和D,而且B和D的物质的量之比为1:1。根据以上事实,写出化学式:A是,B是,C是,D是。加热固体A发生反应的化学方程式为。
(5分).利用右图所示装置收集以下6种气体
(图中烧瓶的位置不得变化):
①NO②Cl2③SO2 ④HCl ⑤NH3
⑴若烧瓶充满水,可收集的气体有,这时气体由口进入(填序号)
⑵若烧瓶是干燥的,则由A口进气,可收集的气体有。
⑶若在烧瓶中装入浓硫酸进行气体干燥,这时气体由口进入,则不可用此装置来干燥的气体有。
(10分)W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生盐和水,该反应的离子方程式为。
(2)W与Y 可形成化合物W2Y,该化合物的电子式为。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为:。
(4)比较Y、Z气态氢化物的稳定性>(用分子式表示)
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是:>>>。
(6分)元素在周期表中的位置,反映了元素的原子结构和元素的性质。右图是元素周期表的一部分。
| C |
N |
O |
F |
||
| Si |
P |
S |
Cl |
||
| Ge |
As |
Se |
Br |
||
| Sn |
Sb |
Te |
I |
||
| Pb |
Bi |
Po |
At |
(1)非金属性最强的元素是,常用来做半导体材料的元素是;
(2)形成化合物种类最多的元素是,写出该元素最高价氧化物的化学式;
(3)根据元素周期律,请你预测(填“>”或“<”):酸性强弱H3AsO4H3PO4,气态氢化物的稳定性AsH3H2Se 。
下列变化(填英文字母)
| A.碘的升华 | B.氯化钠溶于水 | C.氯化氢溶于水 | D.氯化铵受热分解。 |
(1)未发生化学键破坏的是;(2)仅发生离子键破坏的是__________ ;(3) 既发生离子键又发生共价键破坏的是____;