下列有关化学用语的表示正确的是
A.中子数为20的氯原子符号为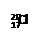 |
| B.乙烯的结构简式为CH2CH2 |
| C.C60和石墨互为同位素 |
| D.NaHCO3的电离方程式为NaHCO3=Na++ HCO3- |
木质素是制浆造纸工业的副产物,具有优良的物理化学特点,若得不到充分利用,变成了制浆造纸工业中的主要污染源之一,不仅造成严重的环境污染,而且也造成资源的重大浪费。木质素的一种单体结构简式如右图所示,下列说法错误的是…………()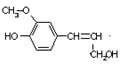
| A.遇FeCl3溶液呈紫色 |
| B.每摩尔该物质最多能消耗4molH2 |
| C.每摩尔该物质最多能消耗3 molBr2 |
| D.该物质的分子式是C10H12O3,不属于芳香烃 |
下列各组中两种气体所含的原子数一定相等的是……………………()
| A.温度相同,体积相同的O2和N2 | B.质量相等,密度不等的N2和CO |
| C.体积相等,密度相等的CO和C2H4 | D.压强相同、体积相同的N2和O2 |
下列离子方程式书写正确的是()
| A.澄清石灰水与少量小苏打溶液混合:Ca2+ + 2OH- + 2 HCO3- →CaCO3↓+ CO32- + 2H2O |
| B.向A1C13溶液中加入过量的氨水:Al3++4NH3·H2O→AlO2-+ 4NH4+ + 2H2O |
| C.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-→CO32-+H2O |
| D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全: |
Ba2+ + 2OH- + NH4+ + H+ + SO42- → BaSO4↓+ NH3·H2O + H2O
据美国《科学》杂志报道,外太空的某个星球的大气层中含有大量的CH2=CHOH,此物质常温下为液体,不稳定,易转化为CH3CHO,方程式为CH2=CHOH→CH3CHO+Q(Q﹥0)。据此,以下叙述中不正确的是……………………………………()
| A.该星球表面温度很低 |
| B.低温下稳定性:CH2="CHOH" < CH3CHO |
| C.该星球表面温度很高 |
| D.高温下稳定性:CH2="CHOH" > CH3CHO |
常温下,浓度均为0.1mol/L的三种溶液:①CH3COOH溶液②NaOH溶液③CH3COONa溶液,下列说法中不正确的是(忽略混合前后溶液体积变化)…………………()
| A.溶液的pH值:②>③>① |
| B.水电离出的c(OH-):③>①>② |
| C.①和②等体积混合后的溶液:c(CH3COOH)+ c(CH3COO-)=0.1mol/L |
| D.②和③等体积混合后的溶液:c(Na+)+ c(H+)=c(OH-)+c(CH3COO-) |