制备食用碘盐(KIO3)原理之一为:I2+2KClO3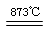 Cl2+2KIO3,下列说法正确的是
Cl2+2KIO3,下列说法正确的是
| A.向KClO3溶液中滴加AgNO3溶液得到白色AgCl沉淀 |
| B.反应过程中I2置换出Cl2,由此可推断非金属性I>CI |
| C.KClO3和KIO3均属于离子化合物,都只含有离子键 |
| D.制备KIO3的反应中氯元素被还原 |
在25oC、1.01×105 Pa下,将2.2 g CO2通入75 mL 1 mol/L NaOH溶液中充分反应,测得反应放出x kJ 的热量.已知在该条件下,1 mol CO2通入1 L 2 mol/L NaOH溶液中充分反应放出y kJ的热量,则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是( )
A.CO2(g)+NaOH(aq)==NaHCO3(aq);ΔH=-(20y-x) kJ/mol
B.CO2(g)+NaOH(aq)==NaHCO3(aq);ΔH=-(4x-y) kJ/mol
C.CO2(g)+NaOH(aq)==NaHCO3(aq);ΔH=-(40x-y) kJ/mol
D.2CO2(g)+2NaOH(l)==2NaHCO3(l);ΔH=-(80x-20y) kJ/mol
已知某可逆反应:mA(g)+nB(g) pC(g) 在密闭容器中进行,下图表示在不同时刻时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是 ()
pC(g) 在密闭容器中进行,下图表示在不同时刻时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是 ()
| A.T2>T1 P1<P2 m+n<P△H<0 | B.T1<T2 P1<P2 m+n<P△H<0 |
| C.T1>T2 P2>P1 m+n>P △H<0 | D.T1>T2 P1<P2 m+n>P △H>0 |
科研人员设想用如图所示装置生产硫酸,下列说法正确的是( )
| A.a为正极,b为负极 | B.生产过程中H+向a电极区域运动 |
| C.电子从b极向a极移动 | D.负极反应式为: |
.以氨气代替氢气来研发氨燃料电池是当前科研的一个热点。氨燃料电池使用的电解质溶液是KOH溶液,电池反应为: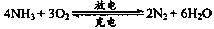
有关下列说法错误的是()
| A.氨燃料电池在放电时,氨气被氧化 |
| B.氨燃料电池在放电时,正极反应为:2NH3+6e-+6OH- |
| C.以氨气代替氢气的主要原因是:氨气易液化易储存 |
| D.燃料电池的能量转化率一般比普通的电池高 |
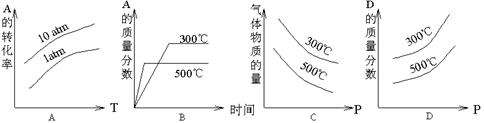
下列表示可逆反应:2A(g)+B(g) 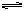 D(g) △H<0的图示中正确的是( )
D(g) △H<0的图示中正确的是( )
(atm压强的一种单位)