下列分子或离子在指定的分散系中能大量共存的一组是
( )
| A.银氨溶液:Na+、K+、NO3—、NH3·H2O |
| B.空气:C2H2、CO2、SO2、NO |
| C.氢氧化铁胶体:H+、K+、S2-、Br- |
| D.高锰酸钾溶液:H+、Na+、SO42—、葡萄糖分子 |
P下列物质呈固态时,一定属于分子晶体的是( )
| A.非金属单质 |
| B.非金属氧化物 |
| C.含氧酸 |
| D.金属氧化物 |
X是核外电子数最少的元素,Y是地壳中含量最丰富的元素,Z在地壳中含量仅次于Y,W可以形成自然界最硬的原子晶体,下列叙述中错误的是( )
| A.WX4是沼气的主要成分 |
| B.固态X2Y是分子晶体 |
| C.ZW是原子晶体 |
| D.玛瑙、水晶和玻璃的成分都是ZY2 |
下列关于晶体的说法一定正确的是()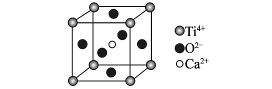
CaTiO3的晶体结构模型(图中Ca2+、O2-、
Ti4+分别位于立方体的体心、面心和顶点)
| A.分子晶体中都存在共价键 |
| B.CaTiO3晶体中每个Ti4+与12个O2-相邻 |
| C.SiO2晶体中每个硅原子与两个氢原子以共价键相结合 |
| D.金属晶体的熔点都比分子晶体的熔点高 |
下列叙述错误的是( )
| A.范德华力是普遍存在的一种分子间作用力,属于电性作用 |
| B.范德华力比较弱,但范德华力越强,物质的熔点和沸点越高 |
| C.氢键属于一种较强的分子间作用力,只能存在于分子之间 |
| D.形成氢键时必须含有氢原子,另外氢原子两边的原子必须具有很强的电负性、很小的原子半径 |
下列有关分子晶体的说法中正确的是( )
| A.分子内均存在共价键 |
| B.分子间一定存在范德华力 |
| C.分子间一定存在氢键 |
| D.其结构一定为分子密堆积 |