下列说法正确的是( )
| A.常温常压下,22.4 L氯气与足量镁粉充分反应,转移的电子数为2NA |
| B.化合反应均为氧化还原反应 |
| C.电解NaCl溶液得到22.4 L H2(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数) |
| D.易燃试剂与强氧化性试剂分开放置并远离火源 |
下列说法不正确的是
| A.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度 |
| B.常温下,向Mg(OH)2饱和溶液中加入NaOH溶液,Mg(OH)2的Ksp不变 |
| C.带有“盐桥”的铜锌原电池比不带“盐桥”的铜锌原电池电流持续时间长 |
| D.对滴加酚酞的NaHCO3溶液加热,红色加深,是因为加热时NaHCO3分解生成Na2CO3,碱性增强 |
已知反应:CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=-41 kJ·mol-1和2H2(g)+O2(g)===2H2O(g) ΔH=-484 kJ·mol-1。则下列说法不正确的是
| A.CO转化为CO2的热化学方程式为2CO(g)+O2(g)===2CO2(g)ΔH=-566 kJ·mol-1 |
B.CO燃烧热的热化学方程式为CO(g)+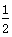 O2(g)===CO2(g) ΔH=-283 kJ·mol-1 O2(g)===CO2(g) ΔH=-283 kJ·mol-1 |
| C.放热反应可能需要加热才能进行,而吸热反应一定需要加热才能进行 |
| D.1mol H2完全燃烧生成1mol 液态水,放出的热量大于242 kJ |
已知同温度下,三种酸的电离平衡常数的大小关系为Ka(HX)>Ka(HY)>Ka(HZ),则物质的量浓度相同的三种盐NaX、NaY和NaZ溶液pH由大到小的顺序是
| A.NaX NaY NaZ | B.NaX NaZ NaY |
| C.NaY NaZ NaX | D.NaZ NaY NaX |
下列叙述中不正确的是
| A.将NaAlO2溶液在蒸发皿中蒸干,最终得到的固体物质是Al(OH)3 |
| B.溶液中c(H+)>c(OH—),该溶液一定显酸性 |
| C.用原电池作电源进行电解时,电子从原电池负极流向电解池阴极 |
| D.外加电流的阴极保护法,构成了电解池;牺牲阳极的阴极保护法构成了原电池 |
某温度下,Kw=10—13,已知该温度下某浓度Na2CO3溶液的pH=10,则该溶液中由水电离的c(OH—)是
| A.1×10—10 mol/L | B.1×10—3 mol/L |
| C.1×10—4 mol/L | D.1×10—7 mol/L |