一定温度下,在某2 L恒容密闭容器中加入纳米级Cu2O并通入0.1 mol H2O(g),发生反应:2H2O(g)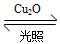 2H2(g)+O2(g) ΔH=+484 kJ·mol-1,不同时间产生O2的物质的量见下表:
2H2(g)+O2(g) ΔH=+484 kJ·mol-1,不同时间产生O2的物质的量见下表:
| 时间/min |
20 |
40 |
60 |
80 |
| n(O2)/mol |
0.001 0 |
0.001 6 |
0.002 0 |
0.002 0 |
下列说法正确的是( )
A.达到平衡时,需要从外界吸收的能量为0.968 kJ
B.前20 min内的平均反应速率v(H2O)=2.5×10-5mol·L-1·min-1
C.增大c(H2O),可以提高水的分解率
D.使用颗粒更小的纳米级Cu2O,可以增大平衡时O2的体积分数
下列图示与对应的叙述相符的是
| A.图1表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 |
| B.图2表示0.1 mol·L-1CH3COOH溶液滴定20.00mL0.1 mol·L-1NaOH溶液所得到的滴定曲线 |
C.图3表示压强对可逆反应2A(g)+2B(g)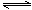 3C(g)+D(s)的影响,乙的压强比甲的压强大 3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| D.据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右 |
下列说法正确的是
| A.AgCl难溶于水,溶液中没有Ag+和Cl- |
| B.自发过程将一定导致体系的熵值增大 |
| C.由能量判据和熵判据组合而成的复合判据,将更适合于所有过程的方向的判断 |
| D.增大反应物的浓度可增大单位体积活化分子百分数,从而使有效碰撞次数增多 |
常温下,下列各组离子,在所给的条件下,一定能够大量共存的是
| A.在c(H+)/c(OH-)=1×1012的溶液中:Fe2+、Mg2+、CO32-、NO3- |
| B.在由水电离出的c(H+)=1×10-12mol/L的溶液中:HCO3-、Al3+、NH4+、ClO- |
| C.在滴加酸碱指示剂酚酞试液后呈现红色的溶液中:Na+、Cl-、AlO2-、CO32- |
| D.在AlCl3溶液中:K+、NO3-、S2-、Na+ |
下列溶液中各微粒的浓度关系不正确的是
| A.0.1 mol/LCH3COOH溶液中:c(CH3COO-)+c(CH3COOH)=0.1mol/L |
| B.NaHCO3溶液中: (OH-) = c(H+) +c(H2CO3)- c(CO32—) |
| C.CH3COONa溶液中:c(Na+)>c(CH3COO-)> (OH-)> c(CH3COOH)> c(H+) |
| D.Na2S溶液中:2c(Na+)= c(S2—) + c(HS—)+ c(H2S) |
下列叙述正确的是
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率;
②镀层破损后,白铁(镀锌铁)比马口铁(镀锡铁)更易腐蚀;
③电镀时,应把镀件置于电解池的阴极;
④ 为防止水闸铁门被腐蚀,可让其与直流电源的负极相连;
⑤放电时溶液中的阴离子向负极移动;⑥甲烷燃料电池,若其电解质溶液是强碱溶液,则其负极反应式:CH4+8OH--8e-=CO2↑+6H2O
| A.①②③④⑤ | B.①③④⑤ | C.①③⑤⑥ | D.③④⑥ |