NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020 mol·L-1的NaHSO3溶液(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55 ℃间溶液变蓝时间,55 ℃时未观察到溶液变蓝,实验结果如下图。据图分析,下列判断不正确的是( )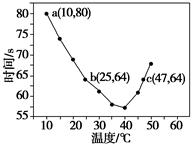
| A.40 ℃之前与40 ℃之后溶液变蓝的时间随温度的变化趋势相反 |
| B.图中b、c两点对应的NaHSO3反应速率相等 |
| C.图中a点对应的NaHSO3反应速率为5.0×10-5 mol·L-1·s-1 |
| D.温度高于40 ℃时,淀粉不宜用作该实验的指示剂 |
(2014届江苏省高三百校联合调研测试(一)化学试卷)
某有机物Z具有较广泛的抗菌作用,其生成机理可由X与Y相互作用: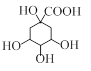
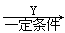

X Z
下列有关叙述中不正确的是
| A.Z结构中有4个手性碳原子 |
| B.Y的分子式为C9H8O3 |
| C.1 mol Z与足量NaOH溶液反应,最多消耗8 mol NaOH |
| D.Z与浓溴水既能发生取代反应又能发生加成反应 |
(届辽宁省东北三省高三第二次模拟考试理综化学试卷)
相对分子质量为100的有机物A能与钠反应,且完全燃烧只生成CO2和H2O。若A含一个六碳环,则环上一氯代物的数目为
| A.5 | B.4 | C.3 | D.2 |
下列化合物的分子中,所有原子都处于同一平面的有
| A.乙烷 | B.甲苯 | C.氟苯 | D.四氯乙烯 |
下列反应中,属于取代反应的是
①CH3CH=CH2+Br2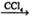 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH2OH 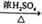 CH2=CH2+H2O
CH2=CH2+H2O
③CH3COOH+CH3CH2OH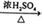 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④C6H6+HNO3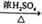 C6H5NO2+H2O
C6H5NO2+H2O
| A.①② | B.③④ | C.①③ | D.②④ |
分子式为C5H11Cl的同分异构体共有(不考虑立体异构)
| A.6种 | B.7种 | C.8种 | D.9种 |