已知298 K时下列物质的溶度积(单位略)。
| |
CH3COOAg |
AgCl |
Ag2CrO4 |
Ag2S |
| Ksp |
2.3×10-3 |
1.77×10-10 |
1.12×10-12 |
6.7×10-15 |
下列说法正确的是( )
A.等体积、浓度均为0.02 mol·L-1的CH3COONa和AgNO3溶液混合能产生沉淀
B.向含有浓度均为0.01 mol·L-1的CrO42—和Cl-的溶液中慢慢滴入AgNO3溶液时,CrO42—先沉淀
C.在CH3COOAg悬浊液中加入盐酸时发生反应的离子方程式为CH3COOAg+H++Cl-=CH3COOH+AgCl
D.298 K时,上述四种饱和溶液的物质的量浓度: c(CH3COOAg)>c(AgCl)>c(Ag2CrO4)>c(Ag2S)
下列观点你认为正确的是()
| A.某单质固体能导电,该单质一定是金属 |
| B.某化合物的水溶液能导电,该化合物一定是电解质 |
| C.某化合物固态不导电,熔融态能导电,该化合物很可能是离子化合物 |
| D.某纯净物常温常压下为气体,则组成该物质的微粒一定含共价键 |
化学与生活是紧密相联的,下列说法正确的是()
| A.地震灾区用漂白粉消毒,是利用漂白粉溶液的碱性 |
| B.鱼、肉、鸡蛋等富含蛋白质的食品被称为碱性食品,长期缺乏可使尿液偏酸性 |
| C.生铁在潮湿的空气中易生锈,其负极反应式为2H2O+O2+4e—===4OH— |
| D.实验室储存的镁条着火时,不可以用泡沫灭火器灭火 |
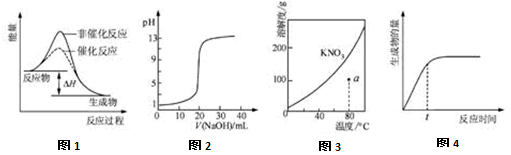
下列图示与对应的叙述相符的是()
| A.图1表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B.图2表示0.1000 mol·L-1NaOH溶液滴定20.00mL0.1000 mol·L-1CH3COOH溶液所得到的滴定曲线 |
| C.图3表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
| D.图4 表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时反应物转化率最大 |
某小组为研究电化学原理,设计如图装置。下列叙述不正确的是()
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu |
| C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D.a和b分别连接直流电源正、负极时,Cu2+向铜电极移动 |
常温下,把1mL0.1mol/L的H2SO4加水稀释到2L溶液,在此溶液中由水电离产生的H+浓度接近于 ( )
| A.1.0×10-4mol/L | B.1.0×10-8mol/L | C.1.0×10-11mol/L | D.1.0×10-10mol/L |