已知常温下CH3COOH的电离平衡常数为Ka。常温下,向20 mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1 NaOH溶液,其pH变化曲线如图所示(忽视温度变化)。下列说法中错误的是( )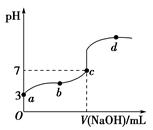
| A.a点表示的溶液中由水电离出的H+浓度为1.0×10-11 mol·L-1 |
| B.b点表示的溶液中c(CH3COO-)>c(Na+) |
| C.c点表示CH3COOH和NaOH恰好反应完全 |
D.b、d点表示的溶液中 相等 相等 |
下列分离提纯方法不正确的是
| A.除去酒精中的水,先加生石灰再用蒸馏法 |
| B.分离碘和氯化钠,用升华法 |
| C.分离四氯化碳和酸性高锰酸钾溶液,用分液法 |
| D.分离KNO3和氯化钠,用过滤法 |
同温同压下,等质量的下列气体所占体积最大的
| A.NH3 | B.H2S | C.HCl | D.O2 |
下列实验操作中,正确的是
| A.测定溶液pH时,用洁净的玻璃棒蘸取待测液点在pH试纸上,观察试纸的颜色变化,并与标准比色卡比较 |
| B.称量NaOH固体时,将NaOH固体放在垫有滤纸的托盘上 |
| C.稀释浓H2SO4时,将蒸馏水沿容器内壁缓慢倒入浓H2SO4中,并及时搅拌 |
| D.在蒸发NaCl溶液得到NaCl晶体的实验中,必须待蒸发皿中的水分全部蒸干后才能撤去酒精灯 |
下列各组微粒中,核外电子总数相等的是
| A.Na+和Li+ | B.H2O和H3O+ | C.CO和CO2 | D.NO和CO |
人类对原子结构的认识经过了一个漫长而曲折的过程,其中提出原子核外的电子是在一系列稳定的轨道上分层运动的是
| A.玻尔 | B.道尔顿 | C.汤姆生 | D.卢瑟福 |