核糖是合成核酸的重要原料,结构简式为CH2OH—CHOH—CHOH—CHOH—CHO。下列关于核糖的叙述正确的是( )
| A.与葡萄糖互为同分异构体 |
| B.可以与银氨溶液作用形成银镜 |
| C.可以跟氯化铁溶液作用显色 |
| D.可以使紫色石蕊试液变红 |
A、B、C三种短周期元素在元素周期表中的相对位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和为C的质子数,现有以下说法,其中判断正确的组合是()
①B与C均存在同素异形体;②X的种类比Y的多③沸点:A的氢化物小于C的氢化物;④C的最高价氧化物对应水化物能与A的氢化物形成三种盐
A.①②③④ B.②③ C.①②④ D.①④
下列说法不正确的是( )
①质子数相同的粒子一定是同一种元素
②质子数相同且电子数也相同的两种粒子不可能一种是分子,另一种是离子
③电子数相同的粒子不一定是同种元素
④一种元素不可以形成不同的单质
⑤某元素的相对原子质量取整数值就是质量数
| A.②④⑤ | B.①④⑤ | C.②③④ | D.①②③④⑤ |
元素R有如下反应:RO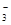 +5R-+6H+===3R2+3H2O,下列说法正确的是()
+5R-+6H+===3R2+3H2O,下列说法正确的是()
| A.元素R位于周期表中第ⅤA族 |
B.RO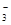 中的R只能被还原 中的R只能被还原 |
C.每反应消耗1 mol RO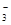 ,转移电子的物质的量为5 mol ,转移电子的物质的量为5 mol |
| D.R2在常温常压下一定是气体 |
下列物质属于分子晶体的是()
| A.熔点是1070℃,易溶于水,水溶液能导电 |
| B.熔点是10.31℃,液态不导电,水溶液能导电 |
| C.能溶于水,熔点812.8℃,沸点是1446℃ |
| D.熔点是97.80℃,质软、导电,密度是0.97g/cm3 |
最近医学界通过用放射性14C标记C60,发现一种C60的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病(AIDS),则有关14C的叙述正确的是()
| A.与C60中普通碳原子的化学性质不同 | B.与14N含的中子数相同 |
| C.是C60的同素异形体 | D.与12C互为同位素 |