用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中不正确的是( )。
| A.X为直流电源的负极,Y为直流电源的正极 |
| B.图中的b>a |
| C.阳极区pH增大 |
| D.该过程中的产品主要为H2SO4和H2 |
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3。则下列说法正确的是
| A.反应过程中,被氧化与被还原的元素的物质的量之比为2:1 |
| B.NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉 |
| C.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染 |
| D.若反应中转移的电子数目为6.02×1023,生成22.4L NO气体 |
常温时,Ksp[Mg(OH)2] = 1.1×10-11,Ksp(AgCl) = 1.8×10-10,Ksp(Ag2CrO4) = 1.9×10-12,Ksp(CH3COOAg) = 2.3×10-3,下列叙述不正确的是
| A.浓度均为0.2 mol·L-1的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀 |
| B.将0.001 mol·L-1的AgNO3溶液滴入0.001 mol·L-1的KCl和0.001 mol·L-1的K2CrO4溶液中,先产生Ag2CrO4沉淀 |
| C.c(Mg2+)为0.11 mol·L-1的溶液中要产生Mg(OH)2沉淀,溶液的pH要控制在9以上 |
| D.在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变 |
下列物质中其电子式可用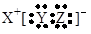 表示的是:
表示的是:
| A.HClO | B.NaHS | C.KOH | D.KClO |
下列依据热化学方程式得出的结论正确的是
| A.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ·mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 |
| B.已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ·mol--1,则氢气的燃烧热为241.8 kJ·mol-1 |
| C.已知2C(s)+2O2(g)=2CO2(g)△H=a、2C(s)+O2(g)=2CO(g)△H=b,则a>b |
| D.已知P (白磷,s)=P (红磷,s)△H<0,则白磷比红磷稳定 |
下列有关实验的操作、原理和现象,正确的是
| A.减压过滤是为了加快过滤速率,得到较大颗粒的晶体 |
| B.硫酸亚铁铵晶体过滤后用无水乙醇洗涤 |
| C.纸层析法分离铁离子和铜离子实验中,展开剂的成份为蒸馏水与丙酮 |
| D.欲分离硝酸钾和氯化钠的混合物(物质的量比为1:1),先将样品溶解,然后加热至表面出现晶膜后冷却,过滤得硝酸钾晶体;将母液加热至大量晶体析出后,用余热蒸干,得氯化钠晶体 |