向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )。
| 选项 |
操 作 |
现 象 |
结 论 |
| A |
某气体遇湿润的淀粉碘化钾试纸 |
试纸变蓝 |
该物质一定是氯气 |
| B |
滴加氯水和苯,振荡、静置 |
上层溶液显紫色 |
原溶液中有I- |
| C |
用洁净铂丝蘸取少量溶液进行焰色反应 |
火焰呈黄色 |
原溶液一定是钠盐溶液 |
| D |
滴加BaCl2溶液 |
产生不溶于稀硝酸的白色沉淀 |
原溶液一定含有Ag+ |
运用元素周期律分析下面的判断,其中错误的是()
| A.铍(Be)的氧化物的水化物可能具有两性 |
| B.砹(At)为白色固体,HAt不稳定,AgAt感光性很强 |
| C.硫酸锶(SrSO4)是难溶于水的白色固体 |
| D.硒化氢(H2Se)无色、有毒,比H2S更不稳定 |
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述正确的是()
| A.常压下五种元素的单质中Z单质的沸点最低 |
| B.Y、Z阴离子电子层结构都与R原子相同 |
| C.W的原子半径比X的小 |
| D.Y元素的非金属性比W元素的非金属性强 |
科学家根据元素周期律和原子结构理论预测,原子序数为114的元素位于第七周期第ⅣA族,称为类铅元素。下面关于它的原子结构和性质的预测正确的是()
| A.类铅元素原子的最外层电子数为6 |
| B.其常见价态为+2、+3、+4 |
| C.它的金属性比铅强 |
| D.它的原子半径比铅小 |
X、Y、Z、W、R是五种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一主族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是()
| A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大 |
| B.元素X不能与元素Y形成化合物X2Y2 |
| C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR |
| D.元素W、R的最高价氧化物对应的水化物都是强酸 |
图中a、b、c、d、e为周期表前四周期的一部分元素,下列叙述正确的是()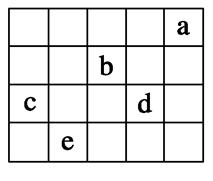
| A.b元素除0价外,只有一种化合价 |
| B.五种元素中,c元素的性质最稳定 |
| C.b、d气态氢化物溶于水,溶液的酸性:b>d |
| D.e元素最高价氧化物的水化物和不同量的氢氧化钠溶液反应,可能生成三种盐 |