某同学用下列装置制备并检验Cl2的性质。下列说法正确的是( )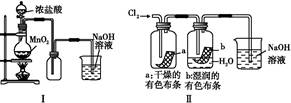

| A.Ⅰ图中:如果MnO2过量,盐酸可全部被消耗 |
| B.Ⅱ图中:湿润的有色布条褪色,证明Cl2有漂白性 |
| C.Ⅲ图中:生成棕色的固体,证明Cl2有强氧化性 |
| D.Ⅳ图中:光照后量筒中气体体积减小,说明甲烷与Cl2发生了加成反应 |
下列排列顺序正确的是
①第一电离能Na<Al<Mg ②热稳定性:H2O>HF>NH3
③酸性:H3PO4>H2SO4>HClO4 ④结合质子能力OH﹣>CH3COO﹣>Cl﹣
⑤还原性:HF<HCl<HBr<HI ⑥离子半径:Ca2+<K+<Cl-<S2-
| A.①②③④ | B.①④⑤⑥ | C.②③④⑤ | D.③④⑤⑥ |
完成下列实验所选择的装置或仪器(夹持装置已略去)不正确的是
| A |
B |
C |
D |
|
| 实 验 |
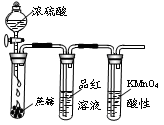
证明浓硫酸有脱水性、强氧化性及SO2有还原性、漂白性 |
用于制取纯净的氢氧化亚铁 |
用于分离NH4Cl和I2的混合物 |
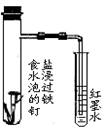
用于证明铁的吸氧腐蚀 |
| 装 置 或 仪 器 |
 |
 |
 |
 |
下列反应的离子方程式书写正确的是
| A.氯化铝溶液中加入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ |
| B.Cu溶于稀硝酸HNO3:Cu+2H++NO3-=Cu2++NO2↑+H2O |
| C.Fe2(SO4)3溶液和Ba(OH)2溶液反应:Fe3++SO42-+Ba2++3OH-=Fe(OH)3↓+BaSO4↓ |
| D.向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
在下列溶液中,各组离子一定能大量共存的是
| A.PH>7的溶液中:K+、AlO2-、Cl-、SO42- |
| B.含有0.1mol/L Fe3+的溶液中:K+、Mg2+、I-、SCN-、HCO3- |
| C.在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3- |
| D.在由水电离产生c(H+)=1×10-13mol/L的溶液中:Na+、S2O32-、 Fe3+、NO3- |
设NA为阿佛加德罗常数的值,下列说法正确的是
| A.常温常压下,8 g O2含有电子数目为4NA |
| B.1 L 0.1mol/L的氯化铵溶液中NH4+的数目为0.1NA |
| C.常温常压下,22.4L氯气与足量的镁粉反应,转移的电子数为2NA |
| D.含1mol FeCl3的饱和溶液滴入沸腾蒸馏水中,所得红褐色液体中含胶粒数目为NA |