将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上并压紧(如图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下表(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大: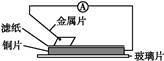
| 金属 |
电子流动方向 |
电压/V |
| 甲 |
甲→Cu |
+0.78 |
| 乙 |
Cu→乙 |
-0.25 |
| 丙 |
丙→Cu |
+1.35 |
| 丁 |
丁→Cu |
+0.30 |
依据记录数据判断,下列结论中正确的是( )
A.将甲、乙形成的合金露置在空气中,甲先被腐蚀
B.金属乙能从硫酸铜溶液中置换出铜
C.在四种金属中丙的还原性最弱
D.甲、丁若形成原电池时,甲为正极
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件关于离子共存说法中正确的是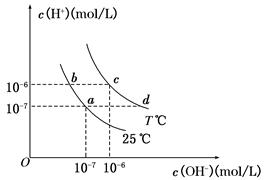
| A.a点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO42- |
| B.b点对应的溶液中大量存在:NH4+.Ba2+、OH-、I- |
| C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、CO32- |
| D.d点对应的溶液中大量存在:Na+、K+、SO32-.Cl— |
下列与金属腐蚀有关的说法正确的是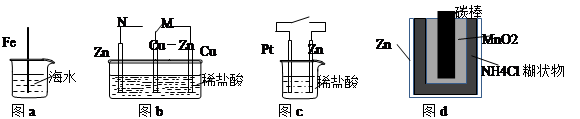
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
绿色电源“二甲醚-氧气燃料电池”的工作原理如下图所示下列说话正确的是:
| A.氧气应从c处通入,电极Y上发生的反应为O2+4e-+2H2O==4OH- |
| B.电池在放电过程中,电极X周围溶液的pH增大 |
| C.二甲醚应从b处加入,电极X上发生的反应为(CH3)2O—12e-+3H2O=2CO2+12H+ |
| D.当该电池向外电路提供2mol电子时消耗O2约为11.2L |
下列判断错误的是
A.沸点: |
B.熔点: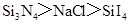 |
C.酸性: |
D.碱性: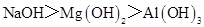 |
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为直线型的共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |