下列实验操作不正确的是( )
| A.用盐酸酸化过的FeCl3溶液,除去H2还原CuO实验中留在试管内的铜 |
| B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| C.蒸馏时,将温度计的水银球靠近蒸馏烧瓶支管口 |
| D.用稀硫酸洗涤长期存放石灰水的试剂瓶 |
下列叙述中不正确的是
| A.“氯碱工业”通过电解饱和食盐水生产氯气和烧碱。 |
| B.通常状况下,干燥的氯气能和Fe反应 |
| C.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照H2和Cl2的混合气体时,因迅速化合而爆炸 |
| D.新制氯水具有漂白性,久置氯水最终变为稀盐酸 |
相同质量的SO2和SO3,下列关系正确的是
| A.含氧原子个数比为2:3 |
| B.含硫元素质量比为4:5 |
| C.含氧元素质量比为5:6 |
| D.含硫原子个数比为1:1 |
向盛有一定量Ba(OH)2溶液中逐滴加入稀硫酸,直至过量,整个过程中混合溶液的导电能力(用电流强度I表示,主要与溶液中可自由移动的离子浓度有关)近似可用下图中的哪条曲线表示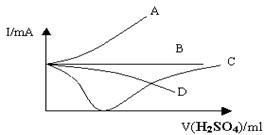
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.18g D2O中含有的氧原子数为NA |
| B.实验室用2mol的浓HCl在加热条件下与足量的MnO2反应,转移的电子数为NA |
| C.22.4L氯化氢溶于水可电离出1molCl- |
| D.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
下列操作中,一定不需要加热的是
| A.萃取 | B.蒸馏 | C.蒸发 | D.溶解 |