氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
(1)根据图1提供的信息,写出该反应的热化学方程式: ,在图1中曲线 (填“a”或“b”)表示加入铁触媒的能量变化曲线。 
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是 。
A.3v(H2)正=2v(NH3)逆
B.单位时间内生成n mol N2的同时生成2n mol NH3
C.混合气体的密度不再改变
D.容器内压强不随时间的变化而变化
(3)一定温度下,向2 L密闭容器中充入1 mol N2和3 mol H2,保持体积不变,0.5 min后达到平衡,测得容器中有0.4 mol NH3,则平均反应速率v(N2)= ,该温度下的平衡常数K= 。若升高温度,K值变化 (填“增大”、“减小”或“不变”)。
(4)为了寻找合成NH3的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
| 实验编号 |
T(℃) |
n(N2)/n(H2) |
p(MPa) |
| ⅰ |
450 |
1/3 |
1 |
| ⅱ |
|
|
10 |
| ⅲ |
480 |
|
10 |
A.请在上表空格中填入剩余的实验条件数据。
B.根据反应N2(g)+3H2(g) 2NH3(g)的特点,在给出的坐标图2中,画出其在1 MPa和10 MPa条件下H2的转化率随温度变化的趋势曲线示意图,并标明各条曲线的压强。
2NH3(g)的特点,在给出的坐标图2中,画出其在1 MPa和10 MPa条件下H2的转化率随温度变化的趋势曲线示意图,并标明各条曲线的压强。
将等物质的量的A、B、C、D四种物质混合,发生如下反应:
aA+bB cC(s)+dD,当反应进行一定时间后,测得A减少了n mol,B减少了
cC(s)+dD,当反应进行一定时间后,测得A减少了n mol,B减少了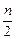 mol,C增加了
mol,C增加了 n mol,D增加了n mol,此时达到化学平衡。
n mol,D增加了n mol,此时达到化学平衡。
(1)该化学方程式各物质的化学计量数为a=__________、b=__________、c=__________、d=__________;
(2)若只改变压强,反应速率发生变化,但平衡不发生移动,该反应中各物质的聚集状态:
A__________、B__________、D__________。
(3)若只升高温度,反应一段时间后,测知四种物质其物质的量又达到相等,则该反应为__________反应(填“放热”或“吸热”)。
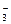
甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是、、。
乙厂的废水中含有另外三种离子。如果加一定量___________ (填“活性炭”“硫酸亚铁”或“铁粉”),可以回收其中的金属___________ (填金属元素符号)。
另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的(填写离子符号)转化为沉淀。经过滤后的废水主要含___________,可用来浇灌农田。
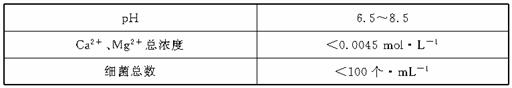
以下是原水处理成自来水的工艺流程示意图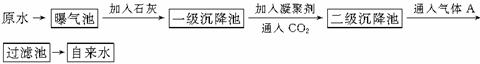
(1)原水中含Ca2+、Mg2+、HCO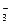 、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式_________________________________
、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式_________________________________
(2)凝聚剂除去悬浮固体颗粒的过程(填写编号,多选倒扣)
①只是物理过程②只是化学过程③是物理和化学过程FeSO4·7H2O是常用的凝聚剂,它在水中最终生成沉淀。
(3)通入二氧化碳的目的是和。
(4)气体A的作用是。这种作用是基于气体A和水反应的产物具有性。
(5)下列物质中,可以作为气体A的代用品。(填写编号)
①Ca(ClO)2 ②浓氨水 ③K2FeO4 ④SO2
(2)在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:_____________________。
在纯碱溶液中滴入酚酞,溶液变红。若在该溶液中再滴入过量的氯化钡溶液,所观察到的现象是___________________________________________,其原因是(以离子方程式和简要文字说明):________________________________