兔耳草醛是食品与化妆品工业中的香料添加剂。工业上可通过有机化工原料A制得,其合成路线如下图所示:
A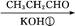 B
B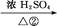 C
C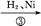 D
D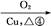
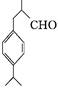 (兔耳草醛)
(兔耳草醛)
已知:①CH3CHO+CH3CHO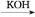 CH3CH(OH)CH2CHO
CH3CH(OH)CH2CHO
②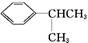 可写成
可写成
(1)B中含氧官能团的名称是 。
(2)上述合成路线中反应①属于 ,反应②属于 (填写反应类型)。
(3)写出由D获得兔耳草醛的化学反应方程式: 。
(4)A的同分异构体中符合以下条件的有 种。
a.能使FeCl3溶液显紫色
b.能发生加聚反应
c.苯环上只有两个互为对位的取代基
从煤中可以获得大量的基本化工原料,苯、二甲苯就是通过煤的干馏而获得的。
(1)苯分子中的氢原子数比同碳原子数的烷烃少,人们认为它是一种不饱和烃。请举出能支持这一观点的一个化学反应(用化学方程式表示):
_____________________________________________________________________。
(2)苯不能使溴水褪色,性质又类似于烷烃,任写一个苯发生取代反应的化学方程式:
_____________________________________________________________________。
(3)二甲苯的分子式为________,与二甲苯互为同分异构体的苯的同系物的名称_______
___________________。
(4)1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释的事实是(填入编号)____________。
| A.苯不能使溴水褪色 | B.苯能与H2发生加成反应 |
| C.溴苯没有同分异构体 | D.邻二溴苯只有一种 |
(5)现代化学认为苯分子中的碳碳键是_______________________________________。
比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理。乙烯和氯化氢在一定条件下制得氯乙烷的化学反应方程式是(有机物用结构简式表示)_____________________________,该反应类型是_____________,该反应的原子利用率为_________,决定氯乙烷能用于冷冻麻醉应急处理的具体性质是___________________________________________________。
(1)体积相同,c(H+)相同的盐酸和醋酸溶液分别与足量的颗粒大小相同的锌粒反应,开始时产生氢气的速率,充分反应后产生氢气的量(相同、醋酸的多、盐酸的多),原因是。
(2)在一定量的盐酸溶液中加入足量的锌粒,要使产生氢气的量保持不变,但反应速率加快,可加入晶体,理由是;要使产生氢气的量不变,但反应速率减慢,可加入晶体,理由是。
可供选择的晶体有:
| A.纯碱 | B.烧碱 | C.胆矾 | D.醋酸钠 E.KHSO4 |
浓度为0.1mol/L的8种溶液:①HNO3 ②H2SO4③HCOOH ④Ba(OH)2 ⑤NaOH ⑥CH3COONa ⑦KCl ⑧NH4Cl溶液pH值由小到大的顺序是(填写编号)____________。
25℃时,将0.01molCH3COONa和0.002molHCl溶于水,形成1L溶液。
(1)该溶液中共含有________种不同的微粒(包括分子和离子);
(2)在这些微粒中,__________和__________两种微粒的物质的量之和等于0.01mol;
(3)________和___________两种微粒的物质的量之和比H+的物质的量多0.008mol。