室温时,甲、乙两同学在实验室配制氯化钠溶液。甲同学配制5%的NaCl溶液100 g,乙同学配制0.5 mol/L的NaCl溶液100 mL(20 ℃时,氯化钠的溶解度为36 g)。下列说法正确的是( )
| A.两同学所需溶质的质量相同 |
| B.两同学所需实验仪器种类相同 |
| C.两同学所配溶液均为不饱和溶液 |
| D.两同学所配溶液的质量相同 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是()
| A.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
| B.标准状况下,22.4L己烷中共价键数目为19NA |
| C.常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
| D.1L浓度为1mol·L-1的Na2CO3溶液中含有NA个CO32- |
在标况下,将V L A气体(摩尔质量M g/mol)溶于1L水中,所得A的水溶液密度为ρg/cm3,则此溶液的物质的量浓度(mol/L)为()
A.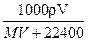 |
B.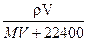 |
C.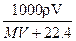 |
D.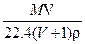 |
下图中有关实验的操作方法或现象有误的是()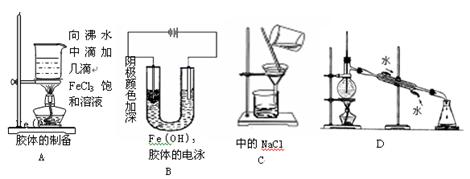
含有分子数为b的某气体质量为a g,则V L标况下的该气体的质量为(式中NA为阿伏伽德罗常数)()
A.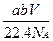 g g |
B. g g |
C.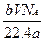 g g |
D.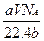 g g |
下列关于溶液和胶体的叙述,正确的是()
| A.溶液是电中性的,胶体是带电的 |
| B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动 |
| C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
| D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有 |