常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关粒子的物质的量变化如图8-2(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )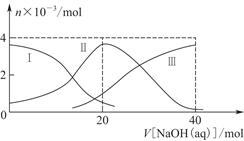
| A.当V[NaOH(aq)]=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| B.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大 |
| C.H2A第一步电离的方程式为H2A=HA-+H+ |
| D.向NaHA溶液加入水稀释的过程中,pH可能增大也可能减小 |
在烷烃同系物中,含碳元素质量分数最大接近于 ( )
| A.75.0% | B.80.0% | C.85.7% | D.92.3% |
某气态烃0.5mol能与1molHCl完全加成,加成后产物分子上的氢原子又可被3molCl2取代,则此气态烃可能是()
| A.CH≡CH | B.CH≡C-CH3 | C.CH2=CH2 | D.CH2=C(CH3)2 |
设阿伏加德罗常数的值为NA,下列说法中正确的是()
| A.1mol苯乙烯中含有的C=C数为4NA |
| B.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| C.0.1molCnH2n+2中含有的C-C键数为0.1nNA |
| D.标准状况下,2.24LCHCl3含有的分子数为0.1NA |
下列物质中含有官能团种类最多的是()
A.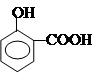 |
B. |
C.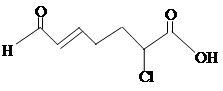 |
D.CH2OH(CHOH)4CHO |
比较乙烷、乙烯、乙炔的组成、结构和性质,不正确的叙述是()
| A.这三种物质都属于气态烃 |
| B.乙炔中碳的质量分数最小 |
| C.溴水能与乙烯和乙炔加成,但不能与乙烷反应 |
| D.一个分子中,共用电子对最多的物质是乙烷 |