纯碱(Na2CO3) 在生产生活中具有广泛的用途。以下是实验室模拟制碱原理制取Na2CO3的流程图:
已知:向饱和食盐水中通入NH3、CO2后发生的反应为NaCl+NH3+CO2+H2O→NaHCO3↓+NH4Cl。请回答以下问题:
(1)粗盐中含有的杂质离子有Ca2+、Mg2+、SO42-等。
精制除杂的步骤顺序a→_______→________→________→b(填字母编号)。
a.粗盐溶解,滤去沉渣;
b.加入盐酸调pH;
c.加入Ba(OH) 2溶液;
d.加入Na2CO3溶液;
e.过滤
向饱和食盐水中先通入NH3,后通入CO2,理由是_____________________。
(2)灼烧固体A制Na2CO3应在_____(填字母序号)中进行。
a.坩埚 b.蒸发皿 c.烧杯 d.锥形瓶
证明滤液A中含有NH4+的方法是 。对滤液A进行重结晶能够获得NH4HCO3,向pH=13含Na+、K+的溶液中加入少量NH4HCO3,使pH降低,反应的离子方程式______________________。
(3)下图装置中常用于实验室制备CO2的是_____(填字母编号);用b示意的装置制备NH3时,分液漏斗中盛放的试剂______(填试剂名称),烧瓶内可加入的固体试剂 (填试剂名称)。
(4)一种天然碱晶体成分是aNa2CO3·bNa2SO4·cH2O,某同学利用下列提供的试剂,设计了如下简单合理测定Na2CO3的质量分数的实验方案。请把实验方案补充完整(仪器自选):
供选择的试剂:1.0 mol·L-1H2SO4溶液、1.0 mol·L-1BaCl2溶液、稀氨水、碱石灰、Ca(OH) 2溶液、蒸馏水
①称取m1 g一定量天然碱晶体样品,溶于适量蒸馏水中;
②_________________________________________________________________;
③_________________________________________________________________;
④计算天然碱晶体中含Na2CO3的质量分数。
(选修)生活中的一些问题常涉及化学知识,下列叙述正确的是
| A.棉花的主要成分是纤维素 |
| B.过多食用糖类物质如淀粉等不会致人发胖 |
| C.淀粉在人体内直接水解生成葡萄糖,供人体组织的营养需要 |
| D.纤维素在人体消化过程中起重要作用,纤维素可以作为人类的营养物质 |
(选修)居室内空气污染物的主要来源是人们使用的装饰材料、胶黏剂、内墙涂料等释放出来的一种有刺激性气味的气体。据此判断,下列说法不正确的是
| A.这种气体是甲醛 |
| B.这种气体是苯 |
| C.该气体可用新制氢氧化铜悬浊液进行检验 |
| D.这种气体可使酸性高锰酸钾溶液褪色 |
(选修)下列食品添加剂与类别对应错误的是()
| A.调味剂——亚硝酸钠 | B.防腐剂——苯甲酸钠 |
| C.疏松剂——碳酸氢钠 | D.着色剂——叶绿素 |
(选修)下列四位同学对“化学与健康”发表的见解中,正确的是()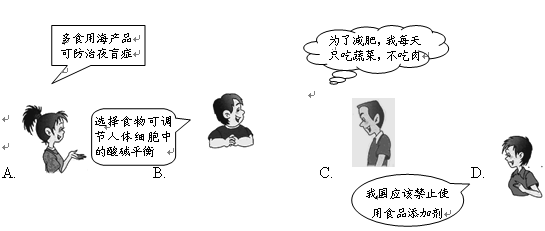
(选修)“垃圾是放错了地方的资源”,应分类回收利用。生活中废弃的塑料袋、废纸、旧橡胶制品等属于()
| A.无机物 | B.有机物 | C.盐类 | D.糖类 |