设NA为阿伏加德罗常数。下列叙述不正确的是
| A.标准状况下,2.24 L Cl2完全溶于足量的水中,转移电子的数目为0.1NA |
| B.常温常压下,11.0g C3H8中含有共价键的数目为2.5NA |
| C.常温常压下,1 L 0.1 mol·L-1 NH4NO3溶液中NO3-的数目为0.1NA |
| D.30g甲醛(HCHO)和醋酸的混合物中含碳原子数目为NA |
如将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即构成甲烷燃料电池。已知通入甲烷的一极,其电极反应为CH4+10OH--8e-=C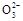 +7H2O,下列叙述正确的是( )。
+7H2O,下列叙述正确的是( )。
| A.通入甲烷的一极为正极 |
| B.通入氧气的一极发生氧化反应 |
C.该电池总反应为CH4+2O2+2OH-=C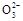 +3H2O +3H2O |
| D.该电池在工作时,溶液中的阴离子向正极移动 |
下列说法正确的是( )。
| A.构成原电池正极和负极的材料必须是金属 |
| B.在原电池中,电子流出的一极是负极,该电极被还原 |
| C.实验室欲快速制取氢气,可利用粗锌与稀硫酸反应 |
| D.原电池可以把物质内部的能量全部转化为电能 |
为将反应2Al+6H+=2Al3++3H2↑的化学能转化为电能,下列装置能达到目的的是(铝条均已除去了氧化膜)( )。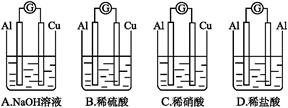
铅蓄电池的两极分别为Pb、PbO2,电解液为硫酸,工作时的反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,下面结论正确的是( )。
| A.Pb为正极,被氧化 |
| B.溶液的pH不断减小 |
C.S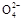 只向PbO2处移动 只向PbO2处移动 |
| D.电解液密度不断减小 |
关于化学电源的叙述,错误的是( )。
| A.化学电源均是根据原电池的工作原理设计的 |
| B.在干电池中,碳棒只起导电作用,并不参加化学反应 |
| C.镍镉电池不能随意丢弃的主要原因是镍、镉的资源有限,价格昂贵 |
| D.燃料电池是一种高效、环保的新型化学电源 |