液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述不正确的是
| A.电流从右侧电极经过负载后流向左侧电极 |
| B.负极发生的电极反应式为:N2H4 + 4OH- - 4e - = N2+ 4H2O |
| C.该燃料电池的电极材料应采用多孔导电材料, 以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 |
| D.该燃料电池持续放电时,正极发生氧化反应,PH减小 |
向一体积为2L的恒容密闭容器里充入1 mol N2和4 molH2,在一定温度下发生反应:
N2(g)+3H2(g) 2NH3(g)+Q (Q > 0)
2NH3(g)+Q (Q > 0)
10秒后达到平衡,c(NH3)为0.4mol/L。下列说法正确的是
| A.该反应达平衡时H2的转化率为40% |
| B.降低温度能使混合气体的密度增大 |
| C.向该容器中充入N2,平衡正向移动 |
| D.研发高效催化剂可大大提高N2的转化率 |
下列示意图中,正确的是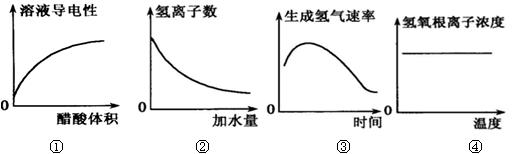
| A.图①表示烧碱溶液中滴加稀醋酸 | B.图②表示稀醋酸加水稀释 |
| C.图③表示镁与一定量的盐酸反应 | D.图④表示加热纯碱溶液 |
下列各组离子在指定溶液中一定能大量共存的是
①澄清透明溶液中:K+、Na+、MnO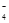 、SO
、SO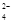
②石蕊呈蓝色的溶液中:Na+、Al3+、NO 、HCO
、HCO
③在pH=1的溶液中:Fe3+、NO 、F -、Na+
、F -、Na+
④含大量OH-的溶液中:CO 、Cl-、F-、K+
、Cl-、F-、K+
⑤在pH=0的溶液中:Na+、NO 、SO
、SO 、K+
、K+
⑥常温下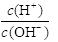 =1012的溶液中:Na+、Al3+、NO
=1012的溶液中:Na+、Al3+、NO 、Cl-
、Cl-
| A.①③④⑤ | B.④⑥ | C.①④⑥ | D.④⑤⑥ |
下列离子方程式正确的是
| A.硝酸银溶液与铜:Cu+Ag+ → Cu2++Ag |
| B.氧化铜与盐酸反应:O2-+2H+ → H2O |
| C.碳酸钡与盐酸:CO32-+2H+ → H2O+CO2↑ |
| D.Cu(OH)2加入H2SO4:2H++Cu(OH)2→ Cu2+ +2H2O |
设NA是阿伏加德罗常数的数值,下列说法正确的是
| A.1molAl3+离子含有的核外电子数为3NA |
| B.1molCl2与足量的铁反应,转移的电子数为3NA |
| C.10LpH=1的硫酸溶液中含有的H+离子数为2NA |
| D.10LpH=13的NaOH溶液中含有的OH-离子数为NA |