脱水环化是合成生物碱类天然产物的重要步骤,某生物碱合成路线如下:
(1)化合物Ⅲ的化学式为 。
(2)化合物A的结构简式为 。
(3)反应①的化学方程式为 。
(4)下列说法错误的是 。
| A.化合物Ⅱ能发生银镜反应 | B.化合物Ⅰ~Ⅴ均属于芳香烃 |
| C.反应③属于酯化反应 | D.化合物Ⅱ能与4 molH2发生加成反应 |
E.化合物Ⅰ、Ⅱ、Ⅲ均能与金属钠反应放出氢气
(5)化合物Ⅵ与化合物Ⅲ互为同分异构体,Ⅵ中含有酯基,且能与FeCl3溶液发生显色反应,其苯环上的一氯代物只有2种。写出一种满足上述条件的Ⅵ的结构简式: 。
(6)化合物Ⅶ如图所示,在一定条件下也能发生类似上述第④步的环化反应,化合物Ⅶ环化反应产物的结构简式为 。
在1.00 L 1.00 mol·L-1 NaOH溶液中通入16.8 L标准状况下的CO2,计算所得溶液中含有NaHCO3和Na2CO3的物质的量。
某地区酸雨经检验除H+和OH-外,还含有Na+、Cl-、NH+4、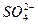 ,其浓度依次为7.0×10-6 mol·L-1,3.5×10-5 mol·L-1,2.3×10-5 mol·L-1,2.5×10-6 mol·L-1,则酸雨的pH为_______________。[已知pH=-lgc(H+)]
,其浓度依次为7.0×10-6 mol·L-1,3.5×10-5 mol·L-1,2.3×10-5 mol·L-1,2.5×10-6 mol·L-1,则酸雨的pH为_______________。[已知pH=-lgc(H+)]
一定量的氢气在氯气中燃烧,所得混合物用100 mL 3.00 mol·L-1的NaOH溶液(密度为1.12 g·mL-1)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.050 0 mol。
(1)原NaOH溶液的质量分数为__________________。
(2)所得溶液中Cl-的物质的量为______________mol。
(3)所用氯气和参加反应的氢气的物质的量之比n(Cl2)∶n(H2)=______________。
(11分)物质的分类方法有多种。如根据同一种物质可能属于不同类别进行分类,也可用归纳、比较等方法对物质进行分类等,完成下列题目。
(1)现有①氧气、②空气、③碱式碳酸铜、④氯酸钾、⑤硫、⑥水、⑦氧化镁、⑧氯化钠、⑨氯水、⑩纯醋酸(CH3COOH)、⑪硫酸钡、⑫乙醇、⑬铜等物质。
其中属于单质的有________,属于化合物的有________,其中________属于含氧化合物,________属于氧化物,属于混合物的有________,属于电解质的是________,属于非电解质的有________(均填序号)。
(2)今有下列两组物质,每组中都有一种物质跟其他三种属于不同的种类。将此种物质和分类依据(选出的物质与其他物质不同之处)写在下面相应的表格内。两组物质分别为:
①O2、Cl2、S、N2
②Fe、Na、Al、Si
| 组别 |
被选出的物质 |
分类依据 |
| 第①组 |
||
| 第②组 |
有一包白色固体,可能含有Na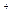 、K
、K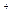 、Ca
、Ca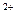 、Cu
、Cu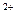 、MnO
、MnO 、Cl
、Cl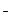 、CO
、CO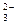 ,现做如下实验:
,现做如下实验:
①将少量固体放入水中,搅拌,静置,得无色溶液且底部有白色沉淀。
②过滤,向沉淀中加盐酸,沉淀全部溶解并产生气体。
③取少量滤液,加入AgNO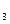 溶液有白色沉淀产生,再加稀HNO
溶液有白色沉淀产生,再加稀HNO ,沉淀部分溶解并有气体放出。
,沉淀部分溶解并有气体放出。
请完成下列问题:
(1)白色固体一定含有的离子是________,一定没有的离子是_____________。
(2)白色固体中可能含有的离子是______________,如检验其是否存在,还需进行的实验操作是__________________________________________。