下列说法正确的是 ( )。
| A.金属元素和非金属元素间形成的化学键一定是离子键 |
| B.ⅦA族元素是同周期元素中非金属性最强的元素 |
| C.全部由非金属元素形成的化合物一定是共价化合物 |
| D.短周期中,同周期元素的离子半径从左到右逐渐减小 |
厦门大学郑兰荪院士合成了C70Cl10富勒烯足球状分子,如下图,它是由C70分子与Cl2发生加成反应得到的。在C70分子中每个碳原子均与周围相邻的其他3个碳原子相连,70个碳原子组成若干个正六边形和正五边形,碳均为4价。则有关说法中不正确的是( ) 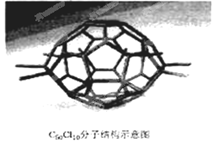
| A.C70的熔点比石墨的熔点低 |
| B.C70分子中的碳原子的杂化方式与碳酸中的碳原子相同 |
| C.C70分子中含有70个σ键,35个π键 |
| D.C70Cl10分子中共用电子对数目为145个 |
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是()
| A.X、Y、Z、W的原子半径依次减小 |
| B.W与X形成的化合物中只含离子键 |
| C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
下列说法正确的是( )
| A.BF3和NF3的空间构型都为平面三角形 |
| B.互为手性异构体的分子的化学式相同 |
| C.熔点:Na-K合金 < 氯化钠 < 钠 << 金刚石 |
| D.空间利用率:体心立方堆积 < 六方最密堆积 < 面心立方最密堆积 |
正硼酸(H3BO3)是一种层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的是( )
| A.正硼酸晶体属于原子晶体 |
| B.H3BO3分子的稳定性与氢键有关 |
| C.分子中硼原子最外层为8e-稳定结构 |
| D.含1mol H3BO3的晶体中有3mol氢键 |
已知某化合物是由钙、钛、氧三种元素组成的晶体,其晶胞结构如图所示,则该物质的化学式为()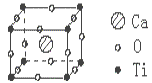
| A.CaTiO3 | B.CaTiO6 | C.Ca4TiO3 | D.CaTiO12 |