电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体。Fe(OH)3有吸附性,可吸附污物使之沉积下来,具有净化水的作用。模拟处理装置如图所示,下列说法错误的是( )
A.X电极是负极,电极反应式为CH4-8e-+4CO32-=5CO2+2H2O |
| B.铁作阳极,失去电子生成Fe2+ |
| C.工作时熔融盐中的碳酸根移向Y电极 |
| D.污水中存在反应4Fe2++10H2O+O2=4Fe(OH)3↓+8H+ |
当2NO2(g) N2O4(g)反应达平衡后,保持其它条件不变,压缩混合气体体积,所观察到的现象是( )
N2O4(g)反应达平衡后,保持其它条件不变,压缩混合气体体积,所观察到的现象是( )
| A.红棕色先变浅后变深最终颜色较浅 |
| B.红棕色先变浅后变深最终颜色较深 |
| C.红棕色先变深后再变浅最终颜色较浅 |
| D.红棕色先变深后变浅最终颜色较深 |
在密闭容器中进行下列反应:A (g)+B (g)  R(g)+2 L此反应符合下面图像。下列叙述正确的是( )
R(g)+2 L此反应符合下面图像。下列叙述正确的是( )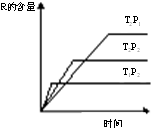
| A.正反应吸热,L是气体 |
| B.正反应放热,L是气体 |
| C.正反应放热,L是液体 |
| D.正反应吸热,L是固体 |
在50ml 0.01mol/L H2SO4溶液加入 50ml 0.01mol/LNaOH溶液时,所得溶液呈
| A.无法判断 | B.碱性 | C.中性 | D.酸性 |
下列叙述正确的是
| A.向0.1 mol/L醋酸溶液中加入少量醋酸钠溶液,溶液的pH增大 |
| B.向0.1 mol/L醋酸溶液中加入少量NaOH溶液,溶液中c(CH3COO-)减少 |
| C.向0.1 mol/L醋酸溶液中不断加水,溶液中c(H+)增大 |
| D.向0.1 mol/L醋酸溶液中滴入少量浓盐酸,溶液的导电性减弱 |
pH=2的强酸溶液,加水稀释,若溶液体积扩大10倍,则C(H+)或C(OH-)的变化
| A.c(H+)和c(OH-)都减少 | B.c(H+)增大 | C.c(OH-)减小 | D.c(H+)减小 |