下列现象或事实可用同一原理解释的是
| A.浓硫酸和浓盐酸长期暴露在空气中浓度均降低 |
| B.氯水和双氧水均要盛装在棕色试剂瓶中 |
| C.SO2能使品红溶液和溴水均褪色 |
| D.NaCl固体中混有NH4Cl或I2,均可用加热法除去 |
元素R有如下反应:RO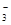 +5R-+6H+===3R2+3H2O,下列说法正确的是()
+5R-+6H+===3R2+3H2O,下列说法正确的是()
| A.元素R位于周期表中第ⅤA族 |
B.RO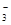 中的R只能被还原 中的R只能被还原 |
C.每反应消耗1 mol RO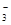 ,转移电子的物质的量为5 mol ,转移电子的物质的量为5 mol |
| D.R2在常温常压下一定是气体 |
下列物质属于分子晶体的是()
| A.熔点是1070℃,易溶于水,水溶液能导电 |
| B.熔点是10.31℃,液态不导电,水溶液能导电 |
| C.能溶于水,熔点812.8℃,沸点是1446℃ |
| D.熔点是97.80℃,质软、导电,密度是0.97g/cm3 |
最近医学界通过用放射性14C标记C60,发现一种C60的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病(AIDS),则有关14C的叙述正确的是()
| A.与C60中普通碳原子的化学性质不同 | B.与14N含的中子数相同 |
| C.是C60的同素异形体 | D.与12C互为同位素 |
下列各组元素中,原子半径依次增大的是:()
A. I、Br、Cl B. Al、Si、P C. O、S、Na D. C、N、B
两种元素原子的核外电子层数之比与最外层电子数之比相等,则在周期表的前10号元素中,满足上述关系的元素共有 ( )
| A.1对 | B.2对 | C.3对 | D.4对 |