粗略测定草木灰中碳酸钾的含量并检验钾元素的存在,需经过称量、溶解、过滤、蒸发、焰色反应等操作。下列图示对应的操作不规范的是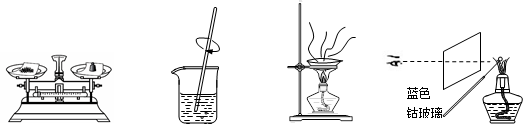
| A.称量 | B.溶解 | C.蒸发 | D.焰色反应 |
下列叙述与盐类水解无关的是
| A.Na2CO3溶液不能盛装在玻璃塞的试剂瓶中 |
| B.饱和食盐水使甲基橙显黄色 |
| C.FeCl3溶液加热蒸干得到Fe2O3 |
| D.0.1mol/LCuCl2溶液中,c(Cu2+)<0.1mol/L |
下列说法正确的是
| A.HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 |
| B.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的2倍 |
| C.室温下,pH=3的亚硫酸溶液中的氢离子浓度与pH=11的氨水中的氢氧根离子浓度相等 |
| D.室温时,将pH=5的H2SO4溶液稀释1000倍,则c(H+):c (SO42-)=2:1 |
120mL含有0.20mol碳酸钠溶液和200mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是
| A.1.2 mol/L | B.2.0mol/L | C.0.18 mol/L | D.0.24mol/L |
CO2与H2的混合气体5g,在150℃时和足量的氧气混合,用电火花充分引燃,在相同状况下,再将反应后所得混合气体通入到足量的Na2O2中,测得Na2O2固体增重的质量为3.4g,则原混合气体中CO2的物质的量分数为
| A.88% | B.75% | C.25% | D.32% |
用1L0.5mol·L-1NaOH溶液吸收0.4molCO2,所以溶液中的CO32-和HCO的物质的量浓度之比约是
| A.1∶3 | B.1∶2 | C.2∶3 | D.3∶1 |