大气中的部分碘源于O3对海水中Iˉ的氧化。将O3持续通入NaI酸性溶液溶液中进行模拟研究。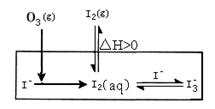
(1)O3将Iˉ氧化成I2的过程可发生如下反应:
①Iˉ(aq)+ O3(g)= IOˉ(aq) +O2(g)△H1
②IOˉ(aq)+H+(aq)  HOI(aq) △H2
HOI(aq) △H2
③HOI(aq) + Iˉ(aq) + H+(aq) I2(aq) + H2O(l) △H3
I2(aq) + H2O(l) △H3
④O3(g)+2Iˉ(aq)+2H+(aq)= I2(aq) + O2(g)+ H2O(l) △H4
则△H3与△H1、△H2、△H4之间的关系是:△H3 = 。
(2)在溶液中存在化学平衡: I2(aq) + Iˉ(aq)  I3ˉ(aq)其平衡常数表达式为 。在反应的整个过程中I3ˉ物质的量浓度变化情况是 。
I3ˉ(aq)其平衡常数表达式为 。在反应的整个过程中I3ˉ物质的量浓度变化情况是 。
(3)为探究温度对I2(aq) + Iˉ(aq) I3ˉ(aq) △H5 反应的影响。在某温度T1下,将一定量的0.2 mol·L-1NaI酸性溶液置于密闭容器中,并充入一定量的O3(g)(O3气体不足,不考虑生成物O2与 Iˉ反应),在t时刻,测得容器中I2(g)的浓度。然后分别在温度为T2、T3、T4、T5下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得I2(g)浓度,得到趋势图(见图一)。则:
I3ˉ(aq) △H5 反应的影响。在某温度T1下,将一定量的0.2 mol·L-1NaI酸性溶液置于密闭容器中,并充入一定量的O3(g)(O3气体不足,不考虑生成物O2与 Iˉ反应),在t时刻,测得容器中I2(g)的浓度。然后分别在温度为T2、T3、T4、T5下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得I2(g)浓度,得到趋势图(见图一)。则: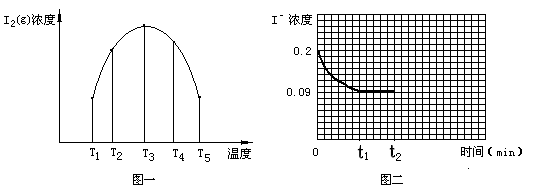
①若在T3时,容器中无O3, T4~T5温度区间容器内I2(g)浓度呈现如图一所示的变化趋势,则△H5 0(填>、=或<);该条件下在温度为T4时,溶液中Iˉ浓度随时间变化的趋势曲线如图二所示。在t2时,将该反应体系温度上升到T5,并维持该温度。请在图2中画出t2时刻后溶液中 Iˉ浓度变化总趋势曲线。
②若在T3时,容器中还有O3,则T1~T2温度区间容器内I2(g)浓度呈现如图一所示的变化趋势,其可能的原因是 。(任写一点)
(4)利用反应④和图2的信息,计算0-t1时间段内用I2(aq)表示的化学反应速率 。
(10分)科学家用NaNO3和Na2O在一定条件下化合制得晶体A,A由钠离子和某阴离子B构成, 则:
(1)A的化学式为,
(2)A对CO2特别敏感,与CO2反应相当剧烈,生成两种常见的物质,该反应的化学方程式为:;
(3)此外,科学家还制备了另一种钠盐D,其与A的组成元素完全相同,D中的阴离子与A中的阴离子表观形式相同(元素种类和原子个数均相同),但D中阴离子的结构中含有一个过氧键:-O-O- ,电导实验表明,同条件下其电导能力与NaCl相同,该阴离子的化学式为,其与水反应生成过氧化氢的离子方程式为 ,该反应(填是或不是)氧化-还原反应
,该反应(填是或不是)氧化-还原反应
已知溶液中:还原性HSO3->I-,氧化性IO3-> I2 > SO42-。在含3 molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示.
试回答下列问题:
(1)写出a点反应的离子方程式_____________________;反应中还原剂是_________;被还原的元素是_________。
(2)写出b点到c点反应的离子方程式________________。
(3)当溶液中的I-为0.4 mol时,加入的KIO3为______mol 。
(4)若往100 mL1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为_______________________。
等质量的两种金属粉末A、B分别与同浓度的足量稀盐酸反应,都生成+2价金属氯化物,其反应情况如图所示:
(1) 两种金属的活动性顺序是_____>______
两种金属氯化物的摩尔质量是_____>______
(2) 将两种金属粉末按一定比例混合后,进行甲、乙丙三组实验,三组实验各取500mL同浓度的盐酸溶液加入该种混合粉末,产生气体,有关数据如下:
| 实验序号 |
甲 |
乙 |
丙 |
| 混合粉末质量(g) |
6.2 |
18.6 |
24.8 |
| 生成气体气体(mL) |
2240 |
5600 |
5600 |
①乙组实验中,盐酸________(填“过量”、“适量”或“不足量”)
②上述所用的盐酸的物质的量浓度为_____mol/L,混合粉末的平均摩尔质量是________。
有机物A可由葡萄糖发酵得到,也可 从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实 验 步 骤 |
解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空: (1)A的相对分子质量为:。 |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现分别增重5.4g和13.2g。 |
(2)A的分子式 为:。 |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 |
(3)用结构简式表示A中含有的官能团: 。 |
(4)A的核磁共振氢谱如下图: |
(4)A中含有种氢原子。 |
| (5)综上所述,A的结构简式。 |
30、酚酞是常用的酸碱指示剂,其结构式如下图所示:
 (1)酚酞的化学式为__________。
(1)酚酞的化学式为__________。
(2)酚酞属于__________ 、__________类衍生物。
、__________类衍生物。