室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
| A.溶液中导电粒子的数目减少 |
B.溶液中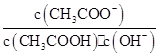 不变 不变 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
| D.再加入10 mL pH=11的NaOH溶液,混合液pH=7 |
下列物质中只含共价键的是
| A.H2O | B.Na2O | C.CaCl2 | D.NH4Cl |
元素的下列性质,随着原子序数的递增不呈周期性变化的是
| A.单质的物理性质 | B.化合价 |
| C.原子半径 | D.元素金属性、非金属性 |
环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动中过度排放有关物质引起的。下列环境问题与所对应的物质不相关的是
| A.温室效应——二氧化碳 | B.光化学烟雾——二氧化氮 |
| C.酸雨——二氧化碳 | D.臭氧层破坏——氟氯烃 |
如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片。经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面。以下有关解释合理的是
| A.生铁片中的碳是原电池的负极,发生还原反应 |
| B.雨水酸性较强,生铁片始终发生析氢腐蚀 |
| C.墨水液面回升时,生铁片发生吸氧腐蚀 |
| D.U型管中溶液pH逐渐减小 |
用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是
| A.稀NaOH溶液 | B.HCl溶液 |
| C.酸性MgCl2溶液 | D.酸性AgNO3溶液 |