有关元素X、Y、Z、W的信息如下:
| 元素 |
有关信息 |
| X |
原子半径为0.074 nm,其氢化物的结构模型可表示为: |
| Y |
原子半径为0.102 nm,其原子核外电子排布为: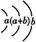 |
| Z |
人体中必需微量元素中含量最多,体内缺失会引起贫血 |
| W |
所在主族序数与所在周期序数之差为4 |
请回答下列问题:
(1)W在元素周期表中的位置是 。
(2)Y与W相比,非金属性较强的是 (填元素符号),下列事实能证明这一结论的是 (填字母)。
a.W元素氢化物的稳定性大于Y元素氢化物的稳定性
b.W元素氢化物水溶液的酸性强于Y元素氢化物水溶液的酸性
c.W元素的单质能与Y元素的氢化物反应,置换出Y单质
d.W的最高价含氧酸比Y的最高价含氧酸的酸性强
(3)Z元素和X元素可形成离子Z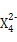 ,含该离子的盐是优良的绿色消毒剂和无机絮凝剂。
,含该离子的盐是优良的绿色消毒剂和无机絮凝剂。
①Z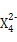 具有强氧化性,能杀菌消毒,还原产物是Z3+。
具有强氧化性,能杀菌消毒,还原产物是Z3+。
②含该离子的盐用作絮凝剂的原因是(用离子方程式和简要的文字说明) 。
已知:R—CH===CH—O—R′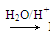 R—CH2CHO+
R—CH2CHO+
(烃基烯基醚)
R′OH,烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3∶4,与A相关的反应如下:
请回答下列问题:
(1)A的分子式为________.
(2)B的名称是________;A的结构简式为________.
(3)写出C―→D反应的化学方程式:______________________________________
________________________________________________________________________.
(4)写出两种同时符合下列条件的E的同分异构体的结构简式:________、________.
①属于芳香烃;
②苯环上有两种不同环境的氢原子.
有机物A为茉莉香型香料
(1)A分子中含氧官能团的名称是____________.
(2)C的分子结构可表示为(其中R和R′代表不同的烃基):
A的化学式是__________,A可以发生的反应是________________(填字母序号).
a.还原反应 b.加成反应 c.氧化反应 d.水解反应
(3)已知含有烃基R的有机物R—OH与浓溴水反应产生白色沉淀,则含有烃基R′的有机物R′—OH的类别属于____________________.
(4)A分子结构中只有一个甲基,A的结构简式是_____________________________
________________________________________________________________________.
关于银镜反应的实验操作步骤如下:
| A.在试管中先注入少量NaOH溶液,振荡,加热煮沸之后把NaOH溶液倒去,再用蒸馏水洗净试管备用. |
| B.在洗净的试管里配制银氨溶液. |
| C.向银氨溶液中滴入3~4滴乙醛稀溶液. |
| D.加热. |
请回答下列问题:
(1)步骤A中加NaOH溶液振荡,加热煮沸的目的是_____________________________
________________________________________________________________________.
(2)简述银氨溶液的配制过程:__________________________________________
________________________________________________________________________.
(3)写出乙醛发生银镜反应的化学方程式:_____________________________________
________________________________________________________________________.
(4)银氨溶液久置可能会爆炸,直接排放会污染环境,且造成资源浪费,实验室从废液中回收银的实验流程如
已知:[Ag(NH3)2]+ Ag++2NH3
Ag++2NH3
①写出废液与稀硝酸反应的离子方程式:__________________________________
________________________________________________________________________.
②加入铁粉要过量的目的是___________________________________________.
③该实验过程中可能产生的大气污染物是________________________________.
有A、B、C三种烃的衍生物,相互转化关系如下: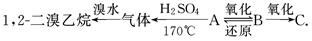
其中B可发生银镜反应,C跟石灰石反应产生能使澄清石灰水变浑浊的气体.
(1)A、B、C的结构简式和名称依次是______________________________________、
________________、________________.
(2)写出下列反应的化学方程式.
①A→B的化学方程式为:_____________________________________________.
②B→C的化学方程式为:_______________________________________________.
③B→A的化学方程式为:______________________________________________.
下图中硬质试管A中放入干燥洁净的细铜丝,烧杯中放入温水,试管B中放入甲醇,右方试管C中放入冷水.向B中不断鼓入空气,使甲醇蒸气和空气通过加热到红热程度的铜丝.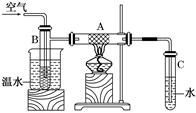
(1)撤去A处酒精灯后铜丝仍然能保持红热的原因是
________________________________________________________________________.
(2)反应后将试管C中的液体冷却,取出少量,加入到新制的Cu(OH)2悬浊液中,加热到沸腾可观察到现象是____________.写出反应的化学方程式_____________________.