用酸性氢氧燃料电池为电源进行电解的实验装置图如图所示,下列说法中正确的是( )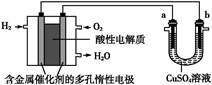
| A.燃料电池工作时,正极反应为:O2+2H2O+4e-=4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4溶液,下列各图中表示其产生氢气总体积(V)与时间(t)的关系正确的是 ( )
COCl2(g)  CO(g)+Cl2(g) △H>0。当反应达到平衡时,下列措施:①升温;②恒压通入惰性气体;③增加CO的浓度;④加催化剂;⑤减压;⑥恒容通入惰性气体。能提高COCl2转化率的是
CO(g)+Cl2(g) △H>0。当反应达到平衡时,下列措施:①升温;②恒压通入惰性气体;③增加CO的浓度;④加催化剂;⑤减压;⑥恒容通入惰性气体。能提高COCl2转化率的是
| A.①④⑥ | B.①②⑤ | C.②③⑥ | D.③⑤⑥ |
在25℃时,密闭容器中X、Y、Z三种气体的浓度如下表: 下列说法错误的是()
下列说法错误的是()
| 物质 |
X |
Y |
Z |
| 初始浓度/mol·L-1 |
0.1 |
0.2 |
0 |
| 平衡浓度/mol·L-1 |
0.05 |
0.05 |
0.1 |
 A.反应达到平衡时,X的转化率为50%
A.反应达到平衡时,X的转化率为50% B.改变温度可以改变此反应的平衡常数
B.改变温度可以改变此反应的平衡常数 C.反应可表示为X+3Y
C.反应可表示为X+3Y 2Z,平衡常数为1600
2Z,平衡常数为1600 D.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.增大压强使平衡向生成Z的方向移动,平衡常数增大
下列说法正确的是()
| A.所有自发进行的化学反应都是放热反应 | B.自发过程将导致体系的熵增大 |
| C.△H-T△S<0反应能自发进行 | D.同一物质的固、液、气三种状态的熵相同 |
在一密闭容器中,反应mA(g)  nB(g)+nC(g)达平衡后,保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,B和C的浓度均是原来的2.2倍,则 ( )
nB(g)+nC(g)达平衡后,保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,B和C的浓度均是原来的2.2倍,则 ( )
| A.物质C的质量分数增加了 | B.物质A的转化率减小了 |
| C.平衡向逆反应方向移动了 | D.m<2n |