甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含离子如下表所示:
| 阳离子 |
NH、Na+、Mg2+ |
| 阴离子 |
OH-、NO3—、SO42— |
取等质量的三种化合物配制相同体积的溶液,其溶质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是( )
①MgSO4 ②NaOH ③(NH4)2SO4 ④Mg(NO3)2 ⑤NH4NO3
A.①② B.③④ C.③⑤ D.①⑤
—种直接肼燃料电池的结构如图所示,下列说法正确的是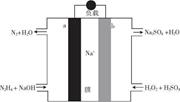
| A.a极为电池的正极 |
| B.电路中每转移6.02X1023个电子,则有1molNa+穿过膜向正极移动 |
C.b极的电极反应式为H202+2e- 20H- 20H- |
| D.用该电池电解饱和食盐水,当阳极生成2.24 L(标准状况)Cl2时,消耗肼0.1 mol |
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数的变化如图所示。已知W的一种核素的质量数为18,中子数为10;X 是短周期元素中原子半径最大的;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法的是不正确的是
| A.简单离子半径:W>X>Z |
| B.最简单气态氢化物的稳定性:Y<Z |
| C.化合物XZW中既含离子键又含共价键 |
| D.Y的氧化物能与X的最高价氧化物对应的水化物反应 |
下列根据实验操作和实验现象所得出的结论不正确的是
下列物质的转化均能通过一步反应实现的是
| A.NaAlO2 A1(OH)3 A1 | B.N2 NO2 HNO3 |
| C.NaOH Na2CO3 NaHCO3 | D.FeS2 S03 H2SO4 |
下列化合物中同分异构体数目(不考虑立体异构)最少的是
| A.分子式为C5 H12的烃经 | B.分子式为C4H100的醇 |
| C.分子式为C4 H8的烯烃 | D.分子式为C3 H602的酯 |