常温下,下列各组离子在指定溶液中能大量共存的是( )
| A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ |
| B.水电离出的c(H+)=10-12 mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+)=0.1 mol/L的溶液中:K+、ClO-、SO42-、SCN- |
25 ℃时,下列各溶液中关系的叙述中,正确的是
| A.pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合, 则c(Na+) + c(H+)=c(OH-) + c(CH3COO-) |
| B.pH=2的盐酸与pH=l的硫酸溶液中c(H+)之比为2∶1 |
| C.0.1 mol/L HA(某酸)溶液pH≠1,0.1 mol/L BOH(某碱)溶液中 c(OH-) =" 0.1" mol/L,则BA(盐)溶液pH<7 |
| D.4种pH相同的溶液①CH3COONa ②C6H5ONa ③NaHCO3④NaOH中c(Na+)的大小顺序是①>②>③>④ |
下列与电化学相关的装置能达到目的的是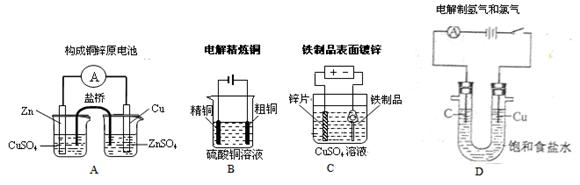
德国科学家格哈德·埃特尔研究的内容能够帮助我们理解铁会生锈、燃料电池如何工作、催化剂如何工作而获得2007年诺贝尔化学奖。下列相关说法正确的是
| A.含碳生铁在发生电化学腐蚀的时,铁做正极 |
| B.C2H6、O2、KOH构成的燃料电池放电一段时间后,负极周围的pH升高 |
| C.CO、O2、KOH构成的燃料电池的负极反应:CO—2e-+4OH-=CO32-+2H2O |
| D.SO2被氧化为SO3时需使用V2O5催化剂,这样可以提高SO2的转化率 |
由水电离出来C(H+)=1×10-12 mol·L-1的无色溶液中,下列离子可能大量共存的是
| A.NH4+、Ba2+、NO3—、CO32— | B.Na+、OH—、SO42—、MnO4— |
| C.K+、Mg2+、NO3-、SO42— | D.Na+、Fe3+、Cl—、AlO2— |
根据化学平衡知识,判断下列说法正确的是
A.已知NaHA溶液呈弱碱性,则该溶液中下列各种微粒浓度大小排列顺序为:
c(Na+)>c(HA-)>c(A2-)>c(H2A)
B.在小苏打溶液中存在下列关系:c(HCO3-) +c (CO32-)+c(H2CO3)=c(Na+)
C.向AgCl悬浊液中加入足量的NaI溶液,会观察到有黄色沉淀生成
D.常温下,稀释0.1 mol/L的氨水,溶液中所有离子浓度均下降