化工生产中含Cu2+的废水常用MnS(s)作沉淀剂,其反应原理为Cu2+(aq)+MnS(s)  CuS(s)+Mn2+(aq)。下列有关该反应的推理不正确的是( )
CuS(s)+Mn2+(aq)。下列有关该反应的推理不正确的是( )
| A.该反应达到平衡时:c(Cu2+)=c(Mn2+) |
| B.CuS的溶解度比MnS的溶解度小 |
| C.往平衡体系中加入少量Cu(NO3)2(s)后,c(Mn2+)变大 |
D.该反应平衡常数表达式:K=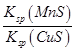 |
下列除去括号内杂质的有关操作方法不正确的是()
| A.乙烷(乙炔):通过盛溴水的洗气瓶 |
| B.乙酸乙酯(乙醇):加入乙酸和浓硫酸的混合液,然后加热 |
| C.苯(苯酚):加入氢氧化钠溶液,然后分液 |
| D.乙醇(水):加入生石灰,然后蒸馏 |
A、B两种烃,它们含碳质量分数相同,下列关于A和B的叙述正确的是()
A.A和B最简式一定相同B.A和B不可能是同系物
C.A和B一定是同分异构体 D.A和B的化学性质相似
研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法错误的是()
| A.萃取是常用的有机物提纯方法 |
| B.燃烧法是研究确定有机物成分的有效方法之一 |
| C.核磁共振氢谱通常用于分析有机物的相对分子质量 |
| D.对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团 |
以下烷烃中,一氯代物只有一种的是()
| A.乙烷 | B.丙烷 | C.2-甲基丁烷 | D.2,2-二甲基丁烷 |
下列有关化学用语正确的是()
①乙烯的最简式C2H4②乙醇的结构简式C2H6O
③四氯化碳的电子式 ④乙炔的结构简式CHCH
④乙炔的结构简式CHCH
⑤乙烷的结构式CH3CH3⑥乙醛的结构简式CH3COH
| A.全对 | B.全错 | C.③④⑤ | D.③④⑥ |