人体血液里存在重要的酸碱平衡: ,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
| c(HCO3-):c(H2CO3) |
1.0 |
17.8 |
20.0 |
22.4 |
| pH |
6.10 |
7.35 |
7.40 |
7.45 |
下列说法不正确的是( )
A.正常人体血液中,HCO3-的水解程度大于电离程度
B.人体血液酸中毒时,可注射NaHCO3溶液缓解
C.pH=7.00的血液中,c(H2CO3)<c(HCO3-)
D.pH=7.40的血液中,HCO3-的水解程度一定大于H2CO3的电离程度
某化合物的结构示意图如下,下列关于该化合物的叙述中正确的是
| A.该化合物只含有H、N、O、Ni四种元素 |
| B.该化合物是配合物,中心离子的配位数是2,配体是氮元素 |
| C.该化合物属于配合物,中心离子是Ni离子 |
| D.该化合物不属于配合物,而是属于高分子化合物 |
元素在周期表中的位置反映了元素的原子结构和元素的性质。下列说法中正确的是
| A.同一元素不可能既表现金属性,又表现非金属性 |
| B.第三周期元素的最高价化合价等于它所处的主族序数 |
| C.短周期元素形成离子后,最外层都达到8电子稳定结构 |
| D.同一主族元素的原子,最外层电子数相同,化学性质完全相同 |
下列分子的空间构型可用sp3杂化轨道来解释的是
①PCl3 ②CH2===CH2 ③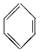 ④CH≡CH ⑤NH3 ⑥CH4
④CH≡CH ⑤NH3 ⑥CH4
| A.①②③ | B.①⑤⑥ | C.②③④ | D.③⑤⑥ |
X元素的价电子结构为ndn+2(n+1)sn-2,则下列判断正确的是
| A.X元素的电子排布式为:1S22S22P63S23P63d104s24p64d65s2 |
| B.X元素位于第五周期 |
| C.X元素位于VIB族 |
| D.X元素原子最外层有2个电子 |
化学中很多“规律”都有其适用范围,据下列 “规律”推出的结论合理的是
| A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 |
| B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
| C.根据价电子构型与元素位置的关系,推出价电子数为3的元素一定在第ⅢA族 |
| D.根据较强酸可以制较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |