化合物H是一种香料,存在于金橘中,可用如下路线合成: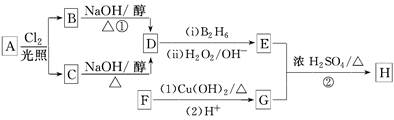
已知:R—CH===CH2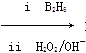 RCH2CH2OH(其中B2H6为乙硼烷)
RCH2CH2OH(其中B2H6为乙硼烷)
请回答下列问题:
(1)11.2 L(标准状况)的烃A在氧气中充分燃烧可以生成88 g CO2和45 g H2O。A的分子式是________________________________________。
(2)B和C均为一氯代烃,它们的名称(系统命名)分别为___________。
(3)在催化剂存在下1 mol F与2 mol H2反应,生成3苯基1丙醇。F的结构简式是___________________________________。
(4)反应①的反应类型是_____________________________。
(5)反应②的化学方程式为__________________________。
(6)与G具有相同官能团的G的芳香类同分异构体共有四种,其中两种分别是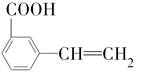 和
和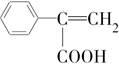 ,另外两种的结构简式分别是___________________________________。
,另外两种的结构简式分别是___________________________________。
【化学——选修3:物质结构与性质】
有A、B、C、D四种元素。已知A原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大。B 的基态原子占据两种形状的原子轨道,且两种形状轨道中的电子总数均相同,B位于元素周期表的s区。C元素原子的外围电子层排布式为nsn-1npn-1。 D原子M能层为全充满状态,且核外的未成对电子只有一个。请回答下列问题:
(1)ACl3分子中A的杂化类型为 。ACl3分子的空间构型为 。
(2)某同学根据上述信息,推断B的核外电子排布如右图所示,
该同学所画的电子排布图违背了 。
(3)A、B、C三元素原子第一电离能由大到小的顺序为 (用元素符号表示)。C60分子中每个原子只跟相邻的3个原子形成共价键,且每个原子最外层都满足8电子稳定结构,则C60分子中π键的数目为 。
(4)D的基态原子有 种能量不同的电子;D2+ 的价电子排布式为 ;下图 (填甲、乙或丙)表示的是D晶体中微粒的堆积方式。若该晶体中一个晶胞的边长为a cm,则D晶体的密度为 (写出含a的表达式,用NA表示阿伏加德罗常数的值)。若D的原子半径为r ,则D晶胞这种堆积模型的空间利用率为 。(用含r的式子表示,不需化简)
甲乙丙
乳酸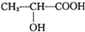 是人体生理活动的一种代谢产物。以下是采用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物。请回答相关问题:
是人体生理活动的一种代谢产物。以下是采用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物。请回答相关问题: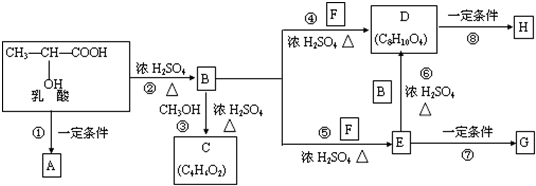
(1)B中所含的官能团有__________、__________;
写出B、C的结构简式:B____________C____________
(2)从下述三个有机基本反应类型中选择指出反应②③所属的类型(填代号):
②____________③____________。
A.取代反应 B.加成反应 C.消去反应
(3)写出下列反应的化学方程式
①_________________⑤_____________________
(4)作为隐形眼镜的制作材料,对其性能的要求除应具有良好的光学性能外,还应具有良好的透气性和亲水性.一般采用E的聚合物G而不是D的聚合物H来制作隐形眼镜,其主要理由是_______________
X、Y、Z三种短周期元素,其中X元素的原子序数大于Y,且X、Y的氧化物都是形成酸雨的主要物质。Z是地壳中含量最高的金属元素;而地壳中含量最高的非金属元素与X同主族、与Y同周期。
(1)实验室用H2XO4制取XO2气体的化学反应方程式为 。(请用具体元素符号表示化学式,下同)
(2)t℃时,0.1 mol·L-1的NaHXO3溶液pH=6,该溶液中各离子浓度由大到小顺序排列为 。
(3)请写出Z的氧化物与烧碱溶液反应的离子方程式 。
(4)一定条件下,YO与YO2存在下列反应:YO(g)+ YO2(g) 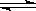 Y2O3(g),其平衡常数表达式为K= 。
Y2O3(g),其平衡常数表达式为K= 。
(5)工业上用氧化YH3法制取YO,该反应的热化学方程式为:
4YH3(g)+5O2(g)=4YO(g)+6H2O(g) △H="-905.8" kJ·mol-1;
已知Y2(g)+O2(g)=2YO(g) △H="+180" kJ·mol-1,则YH3与氧气反应产生两种无污染物质的热化学式为 。
(6)一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其他有机物)。
①导线中电子移动方向为________。(用A、D表示)
②生成目标产物的电极反应式为__________________。
③该储氢装置的电流效率η=____________________。
(η= ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)
A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系: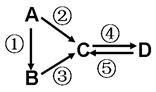
(1)若B是淡黄色固体,②③反应均用到同一种液态氢化物。D物质常用于食品工业。写出④反应的化学方程式 ;
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。写出③反应的化学方程式 ;
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出④反应离子方程式 ;
(4)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中除钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式 ;
(5)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。写出④反应的离子方程式 。
单质Z是一种常见的半导体材料,可由X通过如图所示的路线制备,其中X为Z的氧化物;Y为氢化物,分子结构与甲烷相似,回答下列问题: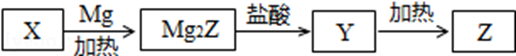
(1)能与X发生化学反应的酸是 ;由X制备Mg2Z的化学方程式为 ;
(2)由Mg2Z生成Y的化学方程式为 ,Y分子的电子式为 。
(3)Z、X中共价键的类型分别是 、 。