下列离子方程式正确的是( )
A.向40 mL 8 mol/L的硝酸溶液中加入5.6 g铁粉:Fe+4H++NO3— Fe3++NO↑+2H2O Fe3++NO↑+2H2O |
B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO- CaSO3↓+2HClO CaSO3↓+2HClO |
C.漂白粉溶液在空气中失效:ClO-+CO2+H2O HClO+HCO3— HClO+HCO3— |
D.Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++2OH-+2H++SO42— BaSO4↓+2H2O BaSO4↓+2H2O |
下列与化学反应能量变化相关的叙述正确的是:
| A.生成物总能量一定低于反应物总能量 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下, H2(g)+ Cl2(g)==="2HCl(g)" 在光照和点燃条件下反应的ΔH不同 |
下面均是正丁烷与氧气反应的热化学方程式(25℃,101 kPa):
①C4H10(g)+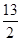 O2(g)===4CO2(g)+5H2O(l)ΔH=-2878 kJ/mol
O2(g)===4CO2(g)+5H2O(l)ΔH=-2878 kJ/mol
②C4H10(g)+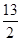 O2(g)===4CO2(g)+5H2O(g)ΔH=-2658 kJ/mol
O2(g)===4CO2(g)+5H2O(g)ΔH=-2658 kJ/mol
③C4H10(g)+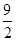 O2(g)===4CO(g)+5H2O(l)ΔH=-1746 kJ/mol
O2(g)===4CO(g)+5H2O(l)ΔH=-1746 kJ/mol
④C4H10(g)+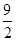 O2(g)===4CO(g)+5H2O(g)ΔH=-1526 kJ/mol
O2(g)===4CO(g)+5H2O(g)ΔH=-1526 kJ/mol
由此判断,正丁烷的燃烧热是:
| A.-2878 kJ/mol | B.-2658 kJ/mol |
| C.-1746 kJ/mol | D.-1526 kJ/mol |
相同状况下:H2(g)+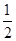 O2(g)===H2O(g) ΔH=-Q1kJ/mol;
O2(g)===H2O(g) ΔH=-Q1kJ/mol;
2H2(g) +O2(g)===2H2O(l) ΔH=-Q2kJ/mol
则Q1和Q2的关系为:
| A.Q1>Q2 | B.Q1=Q2 | C.2Q1<Q2 | D.Q1=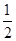 Q2 Q2 |
氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:2H2+4OH—4e-=4H2O O2+2H2O+4e-=4OH-据此作出判断,下列说法中错误的是:
| A.供电时的总反应是:2H2+O2=2H2O | B.产物为无污染的水,属于环境友好电池 |
| C.燃料电池的能量转化率可达100% | D.H2在负极发生氧化反应 |
下列各组材料中,不能组成原电池的是:
| A |
B |
C |
D |
|
| 两极材料 |
Zn片、石墨 |
Cu片、Ag片 |
Zn片、Cu片 |
Fe片、Cu片 |
| 插入溶液 |
稀硫酸 |
硝酸银溶液 |
蔗糖溶液 |
稀盐酸 |