甲醛是一种重要的化工产品,可以利用甲醇脱氢制备,反应式如下:
①CH3OH(g) CH2O(g)+H2(g) ΔH1="+84.2" kJ·mol-1
CH2O(g)+H2(g) ΔH1="+84.2" kJ·mol-1
向反应体系中通入氧气,通过反应②2H2(g)+O2(g) 2H2O(g) ΔH2="-483.6" kJ·mol-1提供反应①所需热量,要使反应温度维持在700 ℃,则进料中甲醇与氧气的物质的量之比约为( )
2H2O(g) ΔH2="-483.6" kJ·mol-1提供反应①所需热量,要使反应温度维持在700 ℃,则进料中甲醇与氧气的物质的量之比约为( )
| A.5.74∶1 | B.11.48∶1 | C.1∶1 | D.2∶1 |
体积为V(mL)、密度为ρ(g·cm-3)的溶液,含有摩尔质量为M的溶质质量为m(g),物质的量浓度为c,质量分数为w。下列表达式中不正确的是
A.c=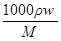 |
B.m=V·ρ·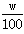 |
C.w=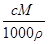 |
D.c=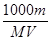 |
下列说法中正确的是
| A.O2的摩尔质量是16g |
| B.碱性氧化物一定是金属氧化物,酸性氧化物一定是非金属氧化物 |
| C.碳酸钠溶液能使酚酞试液变红,因此它是碱 |
| D.虽然二氧化碳溶于水能导电,但它是非电解质 |
下列说法不正确的是
A.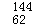 Sm与 Sm与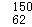 Sm互为同位素 Sm互为同位素 |
| B.氯气能使潮湿的蓝布条变为白色,说明氯气有漂白性 |
| C.将1体积c1mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2c1mol/L |
| D.焰色反应发生的是物理变化 |
一定条件下存在反应:CO(g)+H2O(g) CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换) 密闭容器I、II、III,在I中充入1 mol CO和1 mol H2O,在II中充入1 mol CO2和1 mol H2,在III中充入2 mol CO 和2 mol H2O,700℃条件下开始反应。达到平衡时,下列说法正确的是()
CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换) 密闭容器I、II、III,在I中充入1 mol CO和1 mol H2O,在II中充入1 mol CO2和1 mol H2,在III中充入2 mol CO 和2 mol H2O,700℃条件下开始反应。达到平衡时,下列说法正确的是()
| A.容器I、II中正反应速率相同 |
| B.容器I、III中反应的平衡常数相同 |
| C.容器I中CO 的物质的量比容器II中的少 |
| D.容器I中CO 的转化率与容器II中CO2的转化率之和小于1 |
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g) 2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是()
2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是()
| A.550℃时,若充入惰性气体,ʋ正,ʋ逆均减小,平衡不移动 |
| B.650℃时,反应达平衡后CO2的转化率为 25.0% |
| C.T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 |
| D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数KP=24.0P总 |