可逆反应:A+3B 2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是( )
2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是( )
| A.vD="0.4" mol/(L·s) | B.vC="0.5" mol/(L·s) |
| C.vB="0.6" mol/(L·s) | D.vA="0.15" mol/(L·s) |
19.生活中使用的塑料食品盒、水杯等通常由聚苯乙烯制成,其结构简式为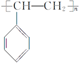 根据所学知识,可以判断
根据所学知识,可以判断
| A.聚苯乙烯能使溴水褪色 |
| B.聚苯乙烯是一种天然高分子化合物 |
| C.聚苯乙烯可由苯乙烯通过化合反应制得 |
| D.聚苯乙烯单体的分子式为C8H8 |
18.下列说法正确的是
| A.乙烯的结构简式可以表示为CH2CH2 |
| B.苯、乙醇和乙酸都能发生取代反应 |
| C.糖类、油脂、蛋白质均为高分子化合物 |
| D.乙酸不能与NaHCO3溶液反应生成CO2 |
17.在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g) + O2(g) = 2CO2(g) △H = —566 kJ/mol
CH4(g) + 2 O2 (g) =" C" O2 (g) + 2H2O(l) △H = —890 kJ/mol
由1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为
| A.2912kJ | B.2953kJ | C.3236kJ | D.3867kJ |
16. 下列各组热化学方程式中,△H1> △H2 的是
①C(s)+O2(g)===CO2(g)△H1C(s)+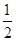 O2(g)===CO(g)△H2
O2(g)===CO(g)△H2
②S(s)+O2(g)===SO2(g)△H1 S(g)+O2(g)===SO2(g)△H2
③H2(g)+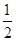 O2(g)===H2O(l)△H12H2(g)+O2(g)===2H2O(l)△H2
O2(g)===H2O(l)△H12H2(g)+O2(g)===2H2O(l)△H2
④CaCO3(s)===CaO(s)+CO2(g)△H1 CaO(s)+H2O(l)===Ca(OH)2(s)△H2
| A.① | B.④ | C.②③④ | D.①②③ |
15.化学反应可视为旧键断裂和新键形成的过程。共价键的键能是两种原子间形成1mol共价键(或其可逆过程)时释放(或吸收)的能量。已知H-H 键的键能为436kJ·mol-1 ,Cl-Cl键的键能为243 kJ·mol-1,H-Cl键的键能为431 kJ·mol-1 ,则H2 (g ) + Cl2 (g ) ="=" 2HCl(g ) 的反应热(△H )等于
| A.-183 kJ·mol-1 | B.183 kJ·mol-1 |
| C.-862 kJ·mol-1 | D.862 kJ·mol-1 |