已知25 ℃时有关弱酸的电离平衡常数如下表:
| 弱酸的化学式 |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数(25 ℃) |
1.8×10-5 |
4.9×10-10 |
K1=4.3×10-7 K2=5.6×10-11 |
则下列有关说法正确的是( )
A.等浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.a mol·L-1 HCN溶液与b mol·L-1 NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于b
C.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离程度、pH均先增大后减小
D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HC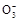 )+2c(C
)+2c(C )
)
下列说法正确的是
| A.瑞典化学家阿累尼乌斯提出了酸碱质子理论,扩大了人们对酸碱的认识 |
| B.活泼金属元素的氧化物一定是碱性氧化物,非金属元素的氧化物一定是酸性氧化物 |
| C.使用太阳能热水器、沼气利用、玉米制乙醇等都涉及到生物质能的利用 |
| D.中国是目前全球最大的稀土提炼和加工国,对稀土元素及其化合物的研究是获得优良催化剂的一种重要途径 |
已知某溶液中含有下列8种离子中的5种(忽略水的电离及离子的水解):K+、Cu2+、Al3+、Fe2+、Cl-、CO32-、NO3-、SO42-,且5种离子的物质的量浓度相等。为了进一步探究该水溶液的组成,某同学进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰。
②另取溶液加入足量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
③另取溶液加入BaCl2溶液,有白色沉淀生成。
根据上述实验,以下推测正确的是____。
| A.无法确定溶液中是否存在Cu2+离子 |
| B.原溶液中不含K+、Al3+、CO32-等离子 |
| C.根据步骤②只能确定溶液中一定存在NO3-离子 |
| D.步骤③所得到的白色沉淀共有2种钡盐 |
根据下表提供的数据,下列判断正确的是
| 弱酸的化学式 |
CH3COOH |
HClO |
H2CO3 |
| 电离平衡常数 |
1.8×10-5 |
3.0×10-8 |
Ka1=4.3×10-7 Ka2=5.6×10-11 |
A.等物质的量的Na2CO3和CH3COOH两种溶液混合,一定有:c(Na+) + c(H+) = 2c(CO32-) + c(HCO3-) + c(CH3COO-)
B.常温下,已知酸H2A存在如下平衡:H2A 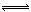 H+ + HA-;HA-
H+ + HA-;HA-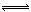 H+ + A2- (Ka15.9×10-2,Ka2=6.4×10-6),则NaHA溶液中水的电离程度一定大于纯水中水的电离程度
H+ + A2- (Ka15.9×10-2,Ka2=6.4×10-6),则NaHA溶液中水的电离程度一定大于纯水中水的电离程度
C.相同浓度的CH3COONa和NaClO混合溶液中各离子浓度大小关系是:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
D.常温下,在0.1mol/LCH3COOH溶液中滴加0.1mol/LNaOH的溶液发生反应,当c(CH3COOH):c(CH3COO-)=5:9时,此时溶液pH=5
用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到某种副产物,其原理如图所示(电极材料为石墨)。下列说法不正确的是
| A.b电极上的主反应是SO32--2e-+H2O==SO42-+2H+ |
| B.若D是混合气体,则可能含有SO2、O2等成分 |
| C.a 电极发生还原反应,当有1mol Na+通过阳离子交换膜时,a极生成11.2L气体 |
| D.A溶液是稀NaOH溶液,作用是增强溶液的导电性;C是较浓的硫酸溶液 |
【改编】下列说法正确的是
A.按系统命名法,化合物 的名称是:2,3-二乙基丁烷 的名称是:2,3-二乙基丁烷 |
| B.已知烃A的分子式为C5Hm,烃B的最简式为C5Hn(m、n均为正整数),则烃A和烃B不可能互为同系物 |
| C.向植物油中加入酸性高锰酸钾紫色溶液,振荡后,酸性高锰酸钾溶液颜色褪去 |
| D.淀粉溶液与稀硫酸溶液共热,再加入新制氢氧化铜悬浊液加热,无红色沉淀,则可证明淀粉没有水解 |