常温下,下列溶液中有关物质的量浓度关系和计算不正确的是
A.c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4Cl溶液中,溶质浓度大小关系是:c(NH4Cl)<c[(NH4)2SO4]<c[(NH4)2Fe(SO4)2]
B.已知25℃时Ksp(AgCl)=1.8×10-10,则在0.1mol·L-1AlCl3溶液中,Ag+的物质的量浓度最大可达到6.0×10-10mol·L-1
C.0.2mol·L-1 HCl溶液与等体积0.05 mol·L-1 Ba(OH)2溶液混合后,溶液的pH="1"
D.室温下,0.1mol?L-1NaHA溶液的pH=4,则有c(HA-)>c(H+)>c(A2-)>c(H2A)
有X、Y、Z、W四种金属。已知X的最高价氧化物的水化物的碱性比Y的强;X3+可使Z氧化;W可与热水反应产生H2,X不能与热水反应;把X的金属片插入稀H2SO4中,让金 属丝Z与X接触,则X的溶解速率加快
属丝Z与X接触,则X的溶解速率加快 。这四种金属活动性强弱关系一定是:
。这四种金属活动性强弱关系一定是:
| A.Y>X | B.Z>Y | C.W>Z | D.Z>X |
哈伯因发明了由氮气和氢气 合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1 mol N2和3 mol H2,在一定条件下使该反应发生,有关说法正确的是
合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1 mol N2和3 mol H2,在一定条件下使该反应发生,有关说法正确的是
N2+3H2 2NH3
2NH3
| A.达到化学平衡时,N2将完全转化为NH3 |
| B.达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 |
| C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 |
| D.达到化学平衡时,正反应和逆反应的速率都为零 |
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲 线如图所示,下列描述正确的是
线如图所示,下列描述正确的是
A.反应开始到10  s,用Z表示的反应速率为 0.158 mol·L-1·s-1
s,用Z表示的反应速率为 0.158 mol·L-1·s-1
B.反应开始到10 s,X的物质的量浓度减少了0.79 mol·L-1
C.反应开始到10 s时,Y的转化率为79.0%
D .反应的化学方程式为:X(g)+ Y(g)
.反应的化学方程式为:X(g)+ Y(g)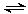 Z(g)
Z(g)
将纯锌片和纯铜片按图示方式插入同浓度同体积的稀硫酸中一段时间,以下叙述正确的是
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.产生气泡的速度甲比乙慢 |
| D.两烧杯中溶液的pH均增大 |
硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,现用以下三种 途径来制取相同质量的硝酸铜:①铜与浓硝酸反应;②铜与稀硝酸反应;③铜与氧气反应生成CuO,CuO再与稀硝酸反应。下列有关叙述正确的是
途径来制取相同质量的硝酸铜:①铜与浓硝酸反应;②铜与稀硝酸反应;③铜与氧气反应生成CuO,CuO再与稀硝酸反应。下列有关叙述正确的是
| A.消耗的硝酸的量:③>①>② |
| B.③对环境造成的危害最小 |
C.因铜与浓硝酸作 用最快,故制取硝酸铜的最佳方案是① 用最快,故制取硝酸铜的最佳方案是① |
| D.三种途径所消耗的铜的质量不相等 |