金属材料在人类生产生活中有着重要的应用,但人们使用更多的不是纯金属,而是合金。
(1)快中子反应堆的热交换剂用的是钠钾合金,其常温下是 态(填气、液、固)。把钠的物质的量分数为20%的0.2mol的此合金安全地加入到重水(D2O)中,产生的气体物质所含的中子数为 。
(2)镁铝合金是经常见到的轻质合金。剪一块合金在空气中燃烧,除生成MgO和Al2O3外,最有可能生成的第三种物质的电子式是 。当一块5.1g的镁铝合金薄片溶于3.6 mol·L-1的200ml 的硫酸溶液中,至少需加入1 mol·L-1的氢氧化钠溶液的体积 mL至沉淀质量不再改变,如整个过程中有0.5mol 的电子发生转移,则合金中Mg的物质的量分数为 。
(3)①有一种铜的合金即黄铜(可看作是Cu和Zn),可分别用酸溶法或碱溶法来分离该两种金属,其中把该合金投入到稀盐酸中,发现产生气泡的速度比用锌与盐酸反应制氢气的速度快,其原因是 。
②为分析某铜合金的成分,用酸将其完全溶解后,用NaOH溶液调pH,当pH=3.4时开始出现沉淀,分别在pH为7.0、8.0时过滤沉淀。结合下图信息推断该合金中除铜外一定含有 。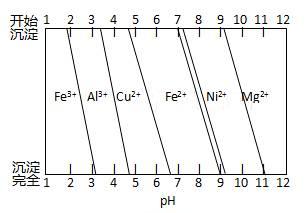
胃酸过多是常见的胃病。下面是甲、乙两种常见胃药的说明摘要。
甲:(1)白色结晶状粉末,可缓缓分解;(2)能溶于水,水溶液呈弱碱性;(3)遇酸或酸性药物则产生二氧化碳;(4)胃酸过多患者服用多见胃胀气,甚至有引起胃溃疡穿孔的危险。
乙:(1)与胃酸是中和作用缓慢而持久,可维持3~4小时。(2)凝胶本身覆盖于溃疡面上,具有保护作用。(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成份是(填化学式);乙中含有的主要化学成份是(填化学式)。
(2)试写出甲中含有的主要化学成份引起胃胀气反应的离子方程式:。
(3)试写出乙中含有的主要化学成份分别与稀盐酸和氢氧化钠溶液反应的离子方程式:。
甲、乙、丙三种物质之间有如下转化关系:
(1)若甲是不溶于水的白色固体物质,既能溶于盐酸又能溶于氢氧化钠溶液,则甲是。
写出“乙 丙”转化的离子方程式:。
丙”转化的离子方程式:。
(2)若乙溶液中加入KSCN溶液,有血红色出现,则甲物质是:。
写出“甲 乙”转化的离子方程式:。.
乙”转化的离子方程式:。.
下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如下图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀。
请回答下列问题:
(1)B中所含元素位于周期表中周期族
请写出C的电子式。
(2)A在B中燃烧的现象是。
(3)D+E→B的反应中,n(被氧化的物质):n(被还原的物质)=。
(4)G+J→M的离子方程式是。
写出C+F→G的离子方程式是。
(5) 受热分解的化学方程式是。
受热分解的化学方程式是。
有关元素X、Y、Z、W的信息如下:
| 元素 |
有关信息 |
| X |
原子半径为0.074 nm,其氢化物的结构模型可表示为: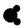 常温下是液体 常温下是液体 |
| Y |
原子半径为0.102 nm,其原子核外电子排布为: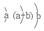 |
| Z |
人体中必需微量元素中含量最多,体内缺失会引起贫血 |
| W |
所在主族序数与所在周期序数之差为4 |
请回答下列问题:
(1)Z在元素周期表中的位置是。
(2)Y与W相比,非金属性较强的是(填元素符号),下列事实能证明这一结论的是(填字母)。
a. W元素氢化物的稳定性大于Y元素氢化物的稳定性
b. W元素氢化物水溶液的酸性强于Y元素氢化物水溶液的酸性
c. W元素的单质能与Y元素的氢化物反应,置换出Y单质
d. W的最高价含氧酸比Y的最高价含氧酸的酸性强
(3)Z元素和X元素可形成离子ZX42-,含该离子的盐是优良的绿色消毒剂和无机絮凝剂。
ZX42-具有强氧化性,能杀菌消毒,还原产物是Z3+,含该离子的盐用作絮凝剂的原因是(用离子方程式和简要的文字说明)。
(14分) 卤化物和卤酸盐在工业生产中有着重要的作用。某小组为探究其中一些盐的性质,查阅资料并进行实验。查阅资料如下:
① BrO3- + 6I- + 6H+ = 3I2 + Br-+ 3H2O② 2BrO3- + I2 = 2IO3- + Br2
③ IO3- + 5I- + 6H+ = 3I2 + 3H2O ④ 2IO3- + 10Br-+ 12H+ = I2 + 5Br2 + 6H2O
实验如下:
| 步骤 |
现象 |
| ⅰ.向盛有30 mL 0.2 mol·L-1 KI溶液的锥形瓶中依次滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液 |
随着KBrO3溶液滴入,溶液由无色变为蓝色并逐渐加深,最终保持不变 |
| ⅱ.继续向上述溶液中滴入KBrO3溶液 |
溶液的蓝色逐渐褪去 |
请回答:
(1)步骤ⅰ开始时发生的反应如资料①所示,溶液中I-完全被氧化时转移mol电子,该反应中硫酸表现出的化学性质是。
(2)上述资料中的反应(填序号)可表示步骤ⅱ中的反应,通过该反应(填“能”或“不能”)说明碘的非金属性强于溴,原因是。
(3)根据资料中的反应①~④并结合所学知识,判断IO3-、BrO3-、I2、Br2的氧化性由强到弱的顺序是;KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是。
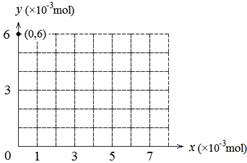
(4)若用y表示锥形瓶中含碘物质的物质的量,用x表示所滴入KBrO3的物质的量,在下图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标)。