1 L K2SO4和CuSO4的混合溶液中c(S )="2.0" mol·L-1,用石墨电极电解此溶液,当通电一段时间后,两极均收集到22.4 L(标准状况)气体,则原溶液中c(K+)为( )
)="2.0" mol·L-1,用石墨电极电解此溶液,当通电一段时间后,两极均收集到22.4 L(标准状况)气体,则原溶液中c(K+)为( )
| A.2.0 mol·L-1 | B.1.5 mol·L-1 |
| C.1.0 mol·L-1 | D.0.5 mol·L-1 |
已知氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1 mol氢气中的化学键消耗的能量为Q1KJ,破坏1 mol氯气中的化学键消耗的能量为Q2KJ,形成1 mol氯化氢中的化学键释放的能量为Q3KJ,则下列关系式中一定正确的是()
| A.Q1+Q2<2Q3 | B.Q1+Q2>2Q3 | C.Q1+Q2<Q3 | D.Q1+Q2=Q3 |
某反应的反应过程中能量变化如右图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是()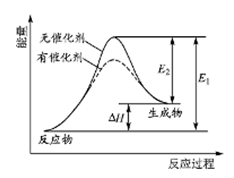
| A.该反应为放热反应 |
| B.催化剂能降低反应的活化能 |
| C.催化剂能改变反应的焓变 |
| D.逆反应的活化能大于正反应的活化能 |
从植物花中可提取一种简写为HIn的有机物,它在水溶液中因存在下列平衡:HIn(溶液,红色)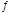 H+(溶液)+In-(溶液,黄色) 而用作酸碱指示剂。往该溶液中加入Na2O2粉末,则溶液颜色为()
H+(溶液)+In-(溶液,黄色) 而用作酸碱指示剂。往该溶液中加入Na2O2粉末,则溶液颜色为()
| A.黄色变浅 | B.红色变深 | C.褪为无色 | D.黄色变深 |
下列冶炼金属的对应关系中错误的是()
| 金属冶炼 |
冶炼方法 |
|
| A |
火烧孔雀石 |
焦炭法 |
| B |
湿法炼铜 |
水煤气法 |
| C |
铝热法炼铬 |
活泼金属置换法 |
| D |
光卤石炼镁 |
电解法 |
某些化学试剂可用于净水。水处理中使用的一种无机高分子混凝剂的化学式可表示为[Al2(OH)nClm·yH2O]X,式中m等于()
| A.6-n | B.3-n | C.6+n | D.3+n |