已知酸性条件下有如下反应:2Cu+ Cu2++Cu。由于反应温度不同,用氢气还原氧化铜时,可能产生Cu或Cu2O,两者都是红色固体。一同学对某次用氢气还原氧化铜实验所得的红色固体产物作了验证,实验操作和实验现象记录如下:
Cu2++Cu。由于反应温度不同,用氢气还原氧化铜时,可能产生Cu或Cu2O,两者都是红色固体。一同学对某次用氢气还原氧化铜实验所得的红色固体产物作了验证,实验操作和实验现象记录如下:
| 加入 试剂 |
稀硫酸 |
浓硫酸、 加热 |
稀硝酸 |
浓硝酸 |
| 实验 现象 |
红色固体和 蓝色溶液 |
无色气体 |
无色气体和 蓝色溶液 |
红棕色气体 和蓝色溶液 |
由此推出本次氢气还原氧化铜实验的产物是( )
A.Cu B.一定有Cu,可能有Cu2O
C.Cu2O D.一定有Cu2O,可能有Cu
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断不正确的是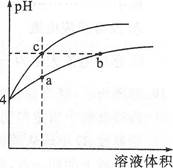
| A.a、b、c三点溶液的Kw相同 |
| B.b点溶液中c(H+)+c(NH3·H2O)=c(OH-) |
| C.用等浓度的NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液的体积Vb>Vc |
| D.a、b、c三点溶液中水的电离程度a>b>c |
如下图所示装置,通入空气,开启a,b两个活塞,灼热铜丝,下列有关分析正确的是
| A.灼热铜丝发生的现象变化为紫红色与黑色交替出现,甲醇发生还原反应 |
| B.C中有机产物易溶于水,与水分子间只形成1种氢键 |
| C.检验C中产物的试剂可用1 mol·L-1的CuS04溶液2 mL和0.4 mol·L-1的NaOH溶液4 mL混合得到 |
| D.可用酸性高锰酸钾溶液检验产物生成 |
化学与生活密切相关.下列说法中不正确的是
| A.“雨后彩虹”是一种与光学和胶体性质相关的自然现象 |
| B.纯银器表面在空气渐渐变暗,是电化学腐蚀所致 |
| C.上图电流表指针偏转,有电流通过 |
| D.在食品中科学使用食品添加剂对人体无害 |
如图所示是四种常见有机物的比例模型示意图。下列说法正确的是
| A.22.4 L甲中含有10 mol电子 |
| B.乙与乙的加聚产物都能使溴水褪色 |
| C.丙不能与溴水、酸性高锰酸钾溶液发生反应 |
| D.丙、丁都可以萃取溴水中的溴单质 |
某二元酸H2A的电离方程式为:H2A=H++HA-;HA- A2-+ H+。下列说法正确的是
A2-+ H+。下列说法正确的是
A.Na2A溶液中:c(Na+)>c(A2-)>c (HA-)>c(H2A)
B.NaHA溶液中:c(Na+)=c(A2-)+c(HA-)
C.Na2A溶液中:c(OH-)=c(H+)+c(HA-)+2c(H2A)
D.室温下0.1mol/L的H2A溶液pH大于1