某实验小组用0.50 mol·L-1NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol·L-1NaOH溶液
(1)若实验中大约要使用470 mL NaOH溶液,至少需要称量NaOH固体 g。
(2)从图中选择称量NaOH固体所需要的仪器是(填字母): 。
| 名称 |
托盘天平 (带砝码) |
小烧杯 |
坩埚钳 |
玻璃棒 |
药匙 |
量筒 |
| 仪器 |
 |
 |
 |
 |
 |
 |
| 序号 |
a |
b |
c |
d |
e |
f |
Ⅱ.测定中和热
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、盐酸、NaOH溶液,尚缺少的实验玻璃用品是 。
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
| 实验 次数 |
起始温度t1/℃ |
终止温度 t2/℃ |
温度差平均值 (t2-t1)/℃ |
|||
| H2SO4 |
NaOH |
平均值 |
||||
| 1 |
26.2 |
26.0 |
26.1 |
30.1 |
|
|
| 2 |
27.0 |
27.4 |
27.2 |
33.3 |
|
|
| 3 |
25.9 |
25.9 |
25.9 |
29.8 |
|
|
| 4 |
26.4 |
26.2 |
26.3 |
30.4 |
|
②近似认为0.50 mol·L-1NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=“4.18”J/(g·℃)。则中和热ΔH= (取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母) 。
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
实验室制取乙烯的装置如下图所示,请回答: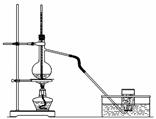
(1)实验室制取乙烯所用的乙醇为无水乙醇,但工业酒精中乙醇的含量为95%,将工业酒精转化为无
水乙醇的方法是。
(2)反应中浓硫酸起和的作用。加热前应该在烧瓶内放入少量碎瓷片,它的作用是。温度计的作用是。
(3)该实验可能产生的主要的有机副产物是。
(4)反应的化学方程式是:反应类型是。
(1)提纯下列物质(括号内为杂质),填写所选用的除杂试剂和除杂方法
| 括号内为杂质 |
除杂试剂 |
操作名称 |
|
| 1 |
乙炔(硫化氢) |
||
| 2 |
溴苯(溴) |
||
| 3 |
苯(苯酚) |
(2)只用一种试剂(可加热)就可区别下列四种无色液体:CH3CH2CH2OH、CH3CH2CHO、HCOOH、CH3COOH,该试剂可以是。
(10分)
某实验需要100 mL、0.1 mol/L的Na2CO3溶液,现通过如下操作配制:
①把称量好的固体Na2CO3放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用(填仪器名称)搅拌
②把①所得溶液冷却到室温后,小心转入(填仪器名称)
③继续加蒸馏水至液面至刻度线1~2cm处,改用(填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切
④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都小心转入容量瓶,并轻轻摇匀
⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序是(填序号)。
(2)若所配溶液的密度为1.06 g/mL,则该溶液的质量分数为。
(3)若取出20 mL配好Na2CO3的溶液,加蒸馏水稀释成c(Na+) ="0.01" mol/L的溶液,则稀释后溶液的体积为mL
(4)在配制100 mL、0.1 mol/L的Na2CO3溶液时,下列操作中的会导致结果偏低(请用
序号填写)
a.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
b.定容时俯视刻度线
c.定容时仰视刻度线
d.干净的容量瓶未经干燥就用于配制溶液
(1)某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。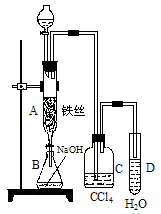
①写出A中有机反应的化学方程式 。
②已知上述有机反应是放热反应,观察到A中的现象是:
及_____ _________。
③ 实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ,写出有关的化学方程式 。
④C中盛放CCl4的作用是 。
⑤能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中滴入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入______ _____,现象是______________________。
(2)乙炔的实验室制法
①反应原理_____ ____________。
②选择合适的制取实验装置___ ___。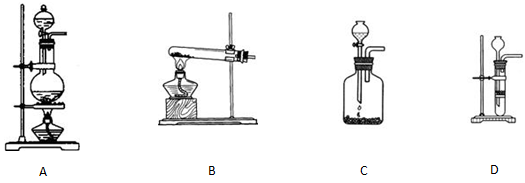
③实验中常用饱和食盐水代替水,目的是______ __________。
④纯净的乙炔气体是无色无味的气体,用电石和水反应制取的乙炔,常含有H2S和PH3而有恶臭气味。可以用____ _______溶液除去杂质气体。
.选择适当的试剂和方法除去下列物质中所含的少量杂质(括号内为杂质):
| 物质 |
试剂 |
方法 |
| (1)乙烷(乙烯) |
||
| (2)溴苯(溴) |
||
| (3)乙醇(水) |
||
| (4)乙酸乙酯(乙酸) |
||
| (5)苯甲酸(NaCl) |